题目内容
现有表面被氧化的镁条样品10g,加入到盛有240.9g10%的稀盐酸的烧杯中,恰好完全反应,得到0.4g气体,则样品中被氧化前镁条的质量分数约为( )
| A、39.4% | B、79.2% |
| C、52% | D、31.2% |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:镁能和空气中的氧气反应生成氧化镁,氧化镁能和稀盐酸反应生成氯化镁和水,镁能和稀盐酸反应生成氯化镁和氢气,表面被氧化的镁条中的镁元素完全转化到氯化镁中,根据稀盐酸的质量、溶质质量分数可以计算氯化镁的质量,进一步可以计算样品中被氧化前镁条的质量分数.
解答:解:设镁元素的质量为x,
240.9g10%的稀盐酸中氯化氢的质量为:240.9g×10%=24.09g,
由Mg+2HCl═MgCl2+H2↑,MgO+2HCl═MgCl2+H2O可知,2HCl~Mg,
2HCl~Mg,
73 24
24.09g x
=
,
x=7.92g,
则样品中被氧化前镁条的质量分数为:
×100%=79.2%,
故选:B.
240.9g10%的稀盐酸中氯化氢的质量为:240.9g×10%=24.09g,
由Mg+2HCl═MgCl2+H2↑,MgO+2HCl═MgCl2+H2O可知,2HCl~Mg,
2HCl~Mg,
73 24
24.09g x
| 73 |
| 24.09g |
| 24 |
| x |
x=7.92g,
则样品中被氧化前镁条的质量分数为:
| 7.92g |
| 10g |
故选:B.
点评:无论是镁,还是氧化镁,和稀盐酸反应时,其中的镁元素都转化到氯化镁中,这是解答的关键,要注意理解.

练习册系列答案
相关题目
下列图示的操作中,正确的是( )
A、 取用药品 |
B、 闻气体气味 |
C、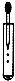 滴加液体 |
D、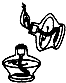 点燃酒精灯 |
关于燃烧和灭火说法正确的是( )
| A、将大块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间 |
| B、火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点 |
C、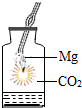 由如图所示可知,金属镁引起的火灾不能用二氧化碳灭火 |
| D、蜡烛用扇子一扇即灭,是因为扇走了蜡烛周围的空气 |
下列化学方程式能正确表示所述内容的是( )
A、铁丝在氧气中燃烧:4Fe+3O2
| ||||
| B、常温下铝与氧气反应:2Al+O2=Al2O3 | ||||
| C、湿法炼铜:2Fe+3CuSO4=Fe2(SO4)3+3Cu | ||||
| D、二氧化碳通入澄清石灰水:CO2+Ca (OH)2=CaCO3↓+H2O |
下列葡萄酿酒中,属于化学变化的是( )
| A、清洗葡萄 |
| B、把葡萄捣碎 |
| C、葡萄发酵成酒 |
| D、用细纱布过虑装瓶 |




