题目内容
10.在一次化学实验操作考核中,某班同学有如下几种操作,其中正确的是( )| A. |  用天平称食盐 用天平称食盐 | B. |  稀释浓硫酸 | C. |  检查气密性 | D. |  过滤 |
分析 A、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
B、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
C、根据检查装置气密性的方法进行分析判断.
D、过滤液体时,注意“一贴、二低、三靠”的原则.
解答 解:A、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作错误.
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作错误.
C、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确.
D、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流、漏斗下端没有紧靠在烧杯内壁上,图中所示操作错误.
故选:C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
3.青少年每天需要摄入充足的蛋白质,下列食物中富含蛋白质的是( )
| A. | 土豆 | B. | 牛肉 | C. | 大黄瓜 | D. | 米饭 |
1.下列实验操作正确的是( )
| A. |  检查装置气密性 | B. |  点燃酒精灯 | C. |  加热液体 | D. |  收集呼出的气体 |
15.已知某金属粉末中除含有Al外还含有一定量的Fe,为测定金属的含量,某化学兴趣小组的同学展开了如下的实验探究.
小资料:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:
2Al+2H2O+2NaOH═2NaAlO2+3H2↑,Fe不与氢氧化钠溶液反应).
取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据如下:
(1)第四次加入NaOH后,溶液中的溶质是氢氧化钠和偏铝酸钠;
(2)Fe的质量分数为30%;
(3)第三次加入氢氧化钠溶液后,共生成多少克氢气?所用氢氧化钠溶液的溶质质量分数为多少?(精确到0.1%)
小资料:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:
2Al+2H2O+2NaOH═2NaAlO2+3H2↑,Fe不与氢氧化钠溶液反应).
取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据如下:
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 剩余固体的质量/g | 16.4 | 12.8 | 9.2 | 6 | m |
(2)Fe的质量分数为30%;
(3)第三次加入氢氧化钠溶液后,共生成多少克氢气?所用氢氧化钠溶液的溶质质量分数为多少?(精确到0.1%)
2.下列物品中是由有机合成材料制成的是( )
| A. |  塑料座椅 | B. |  纯棉衬衫 | C. |  不锈钢杯瓶 | D. |  青花瓷 |
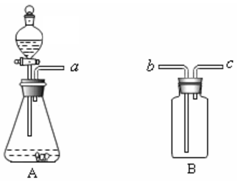 如图实验装置适当组合可用于O2、H2、CO2等气体的制备和收集.
如图实验装置适当组合可用于O2、H2、CO2等气体的制备和收集. 如图是汽车安全气囊打开时的情境.安全气囊中含有叠氮化钠(NaN3)等物质.
如图是汽车安全气囊打开时的情境.安全气囊中含有叠氮化钠(NaN3)等物质.