题目内容
9.向氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,所得的滤液中一定含有的溶质是MgCl2.分析 根据金属活动顺序表知:镁>铁>H>铜,所以加入镁粉,首先镁粉和氯化铜溶液反应,置换出单质铜,如果镁粉足量可以再继续和氯化亚铁反应置换出铁.
解答 解:在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,若镁粉足量,则铜和铁被全部置换出来,溶液中只含有MgCl2;若镁粉的量不足,只能置换出铜,则溶液中含有FeCl2、MgCl2;若镁粉的量很少,只能置换出部分的铜,则溶液中含有FeCl2、MgCl2、CuCl2,由分析可知,一定含有的溶质是MgCl2.
故答案为:MgCl2.
点评 本题主要考查了学生对金属活动顺序表的运用以及半定量(如一定量、过量、少量等)概念的理解和掌握.

练习册系列答案
相关题目
19.下列说法正确的是( )
| A. | 由一种元素的阳离子跟另一种元素的阴离子构成的物质一定是纯净物 | |
| B. | 能跟酸反应生成盐和水的化合物一定是碱 | |
| C. | 最外层电子数小于4的元素一定是金属元素 | |
| D. | 在能导电的溶液里,所有阳离子带的正电荷总数与所有阴离子带的负电荷总数相等 |
14.下列图象中不能正确反映对应关系的是( )


| A. | 电解水 | |
| B. | 将一定量的氯酸钾与二氧化锰混合物加热 | |
| C. | t℃时,向一定量的不饱和硝酸钾溶液中加入硝酸钾固体 | |
| D. | 向一定量的硫酸和硫酸铜混合溶液中不断加氯化钡溶液 |
8.下列生活事例中,属于化学变化的是( )
| A. | 把西瓜榨成汁 | B. | 铁锅生锈 | ||
| C. | 把铁丝弯曲成衣架 | D. | 给自行车胎打气 |
9.NaOH、Ca(OH)2是常见的两种碱,它们具有相似的化学性质,如其溶液都能与CO2反应,但NaOH溶液与CO2反应时没有明显的现象.对此,小希思考:能否让两个反应都能直接观察到明显的现象.
【查阅资料】20℃时,NaOH、Na2CO3、NaCl分别在水、酒精中的溶解度(单位:g/100g 溶剂)
从数据分析可知,物质的溶解度受②(填序号)影响.
①溶剂的质量 ②溶剂的性质 ③溶质的性质 ④温度
【进行实验】
(1)小希按图一所示步骤配制饱和NaOH的酒精溶液.
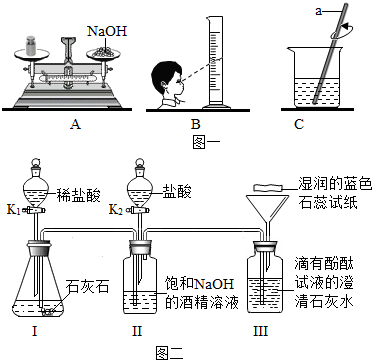
①仪器a的作用是搅拌.
②小希所配制的溶液不是(填“是”或“不是”)饱和溶液.
(2)验证CO2分别与NaOH、Ca(OH)2的反应.
①图二装置I中有一个错误,造成的后果是CD(填序号).
A.漏气 B.不能产生CO2 C.CO2不能进入Ⅱ中 D.装置Ⅰ中胶塞可能被冲出
②改进后,打开K1,关闭K2,Ⅱ中主要现象是产生沉淀,化学反应方程式为CO2+2NaOH═Na2CO3↓+H2O,此时Ⅲ中无现象.
③关闭K1,打开K2,能体现酸的化学性质的反应方程式为HCl+NaOH=NaCl+H2O(写一个).Ⅲ中可观察到澄清石灰水变浑浊,酚酞试液由红色变为无色,润色石蕊试纸变红,
【交流讨论】使润湿石蕊试纸变红的原因是:
A.漏斗中聚集了未反应完的CO2 B.盐酸挥发的氯化氢气体 C.两个原因共同所致
要肯定只是原因A,需补做的实验是:将气体通入碳酸钠溶液中没有气泡生成..
【查阅资料】20℃时,NaOH、Na2CO3、NaCl分别在水、酒精中的溶解度(单位:g/100g 溶剂)
| NaOH | Na2CO3 | NaCl | |
| 水 | 109 | 21.8 | 36.0 |
| 酒精 | 17.3 | 不溶 | 0.1 |
①溶剂的质量 ②溶剂的性质 ③溶质的性质 ④温度
【进行实验】
(1)小希按图一所示步骤配制饱和NaOH的酒精溶液.

①仪器a的作用是搅拌.
②小希所配制的溶液不是(填“是”或“不是”)饱和溶液.
(2)验证CO2分别与NaOH、Ca(OH)2的反应.
①图二装置I中有一个错误,造成的后果是CD(填序号).
A.漏气 B.不能产生CO2 C.CO2不能进入Ⅱ中 D.装置Ⅰ中胶塞可能被冲出
②改进后,打开K1,关闭K2,Ⅱ中主要现象是产生沉淀,化学反应方程式为CO2+2NaOH═Na2CO3↓+H2O,此时Ⅲ中无现象.
③关闭K1,打开K2,能体现酸的化学性质的反应方程式为HCl+NaOH=NaCl+H2O(写一个).Ⅲ中可观察到澄清石灰水变浑浊,酚酞试液由红色变为无色,润色石蕊试纸变红,
【交流讨论】使润湿石蕊试纸变红的原因是:
A.漏斗中聚集了未反应完的CO2 B.盐酸挥发的氯化氢气体 C.两个原因共同所致
要肯定只是原因A,需补做的实验是:将气体通入碳酸钠溶液中没有气泡生成..