题目内容
9.NaOH、Ca(OH)2是常见的两种碱,它们具有相似的化学性质,如其溶液都能与CO2反应,但NaOH溶液与CO2反应时没有明显的现象.对此,小希思考:能否让两个反应都能直接观察到明显的现象.【查阅资料】20℃时,NaOH、Na2CO3、NaCl分别在水、酒精中的溶解度(单位:g/100g 溶剂)
| NaOH | Na2CO3 | NaCl | |
| 水 | 109 | 21.8 | 36.0 |
| 酒精 | 17.3 | 不溶 | 0.1 |
①溶剂的质量 ②溶剂的性质 ③溶质的性质 ④温度
【进行实验】
(1)小希按图一所示步骤配制饱和NaOH的酒精溶液.
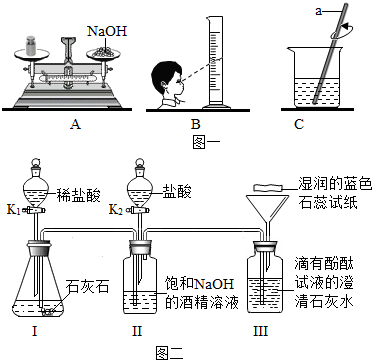
①仪器a的作用是搅拌.
②小希所配制的溶液不是(填“是”或“不是”)饱和溶液.
(2)验证CO2分别与NaOH、Ca(OH)2的反应.
①图二装置I中有一个错误,造成的后果是CD(填序号).
A.漏气 B.不能产生CO2 C.CO2不能进入Ⅱ中 D.装置Ⅰ中胶塞可能被冲出
②改进后,打开K1,关闭K2,Ⅱ中主要现象是产生沉淀,化学反应方程式为CO2+2NaOH═Na2CO3↓+H2O,此时Ⅲ中无现象.
③关闭K1,打开K2,能体现酸的化学性质的反应方程式为HCl+NaOH=NaCl+H2O(写一个).Ⅲ中可观察到澄清石灰水变浑浊,酚酞试液由红色变为无色,润色石蕊试纸变红,
【交流讨论】使润湿石蕊试纸变红的原因是:
A.漏斗中聚集了未反应完的CO2 B.盐酸挥发的氯化氢气体 C.两个原因共同所致
要肯定只是原因A,需补做的实验是:将气体通入碳酸钠溶液中没有气泡生成..
分析 【查阅资料】根据表中的数据分析影响溶解度的因素.
【进行实验】(1)①根据玻璃棒的作用分析回答;
②根据托盘天平、量筒的使用方法分析判断;
(2)①根据装的特点分析产生的后果.
②根据二氧化碳与氢氧化钠反应生成的碳酸钠不溶于酒精分析回答.
③根据盐酸能与氢氧化钠、碳酸钠反应分析体现酸的性质,根据酚酞试液的变色分析颜色的变化;
【交流讨论】二氧化碳、氯化氢气体能使润湿石蕊试纸变红,盐酸能与碳酸钠反应,据此解答.
解答 解:【查阅资料】由表中的数据可知,同一种物质在不同溶剂中的溶解度不同,说明了物质的溶解度受 溶剂性质的影响.
【进行实验】(1)①仪器a的作用是搅拌;
②由图示可知,用托盘天平称量氢氧化钠是左码右物,使用了游码,称量的氢氧化钠偏少,在量取水时仰视度数,实际量取的水偏多,配成的溶液因为不饱和溶液.
(2)①由装置的特点可知看出,导气管伸入到液面以下,产生的气体排不出去,CO2不能进入Ⅱ中,装置Ⅰ中胶塞可能被冲出;
②改进后,打开K1,关闭K2,由于二氧化碳与氢氧化钠反应生成的碳酸钠不溶于酒精,所以Ⅱ中主要现象是产生沉淀,化学反应方程式为:CO2+2NaOH═Na2CO3↓+H2O,此时Ⅲ中无现象.
③盐酸能与氢氧化钠、碳酸钠反应,体现出酸的性质,反应的方程式是:HCl+NaOH=NaCl+H2O等.Ⅲ中可观察到澄清石灰水变浑浊,由于氢氧化钙与二氧化碳反应生成了碳酸钙和水,所以酚酞试液由红色变为无色,润色石蕊试纸变红,
【交流讨论】由于反应生成的二氧化碳,盐酸挥发出的氯化氢气体都能使使润湿石蕊试纸变红.盐酸能与碳酸钠反应生成了气体.可用碳酸钠溶液来判断气体中是否含有氯化氢气体.所以,B应填:盐酸挥发的氯化氢气体.要肯定只是原因A,需补做的实验是:将气体通入碳酸钠溶液中没有气泡生成.
故答为:
【查阅资料】②.
【进行实验】(1)①搅拌;②不饱和;
(2)①CD.
②产生沉淀,CO2+2NaOH═Na2CO3↓+H2O.
③HCl+NaOH=NaCl+H2O;
【交流讨论】盐酸挥发的氯化氢气体.将气体通入碳酸钠溶液中没有气泡生成.
点评 本题通过探究实验考查了二氧化碳、盐酸、氢氧还钙、氢氧化钠的知识,综合性较强,难度较大,只有加强酸、碱、盐等知识的学习才能较好的完成本题.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案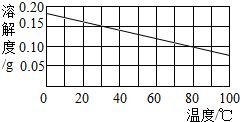 如图是氢氧化钙的溶解度曲线图.现有10℃含l00g水的澄清氢氧化钙饱和溶液.若把该溶液用水浴加热到60℃(水的蒸发忽略不汁).下列说法错误的是( )
如图是氢氧化钙的溶解度曲线图.现有10℃含l00g水的澄清氢氧化钙饱和溶液.若把该溶液用水浴加热到60℃(水的蒸发忽略不汁).下列说法错误的是( )| A. | 溶液变浑浊了 | B. | 溶液中溶质发生了化学变化 | ||
| C. | 溶液仍饱和 | D. | 溶液中溶质质量分数变小 |
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量(g) | 15.0 | 15.0 | 15.0 | 15.0 |
| 剩余固体的质量(g) | 7.0 | M= | 1.0 | 1.0 |
(2)计算样品中碳酸钙的质量分数.
(3)所用稀盐酸溶液的溶质质量分数是多少?(计算结果精确到小数点后一位).
| A. | 过量排放CO2-形成酸雨 | B. | 减少氟利昂的使用-防止臭氧空洞 | ||
| C. | 发展太阳能-开发清洁能源 | D. | 禁止滥砍乱发树木-减缓温室效应 |
| A. | 用木炭除去冰箱里的异味 | |
| B. | 用醋酸洗去水壶中的水垢 | |
| C. | 在煤炉上放一盆水预防煤气中毒 | |
| D. | 用灯火检验地窖中二氧化碳的含量是否超标 |
| A. | 细铁丝在氧气里剧烈燃烧,火星四射 | |
| B. | 镁带燃烧产生发出耀眼的白光 | |
| C. | 蜡烛在空气中燃烧生成二氧化碳和水 | |
| D. | 蘸有浓氨水和浓盐酸的玻璃棒靠近,产生白烟 |