题目内容
2. 如图是实验室检验溶液的酸碱性的实验,请回答下列问题:
如图是实验室检验溶液的酸碱性的实验,请回答下列问题:(1)图中用于滴加指示剂的仪器的名称是胶头滴管,该实验用点滴板代替试管的优点是节约药品.
(2)氢氧化钙、氢氧化钠等碱类物质都能使指示剂变色,是因为不同的碱溶液中都含有相同的OH-.(填微粒符号)
(3)如果使氢氧化钙溶液与碳酸钠溶液混合,可观察到的现象是产生白色沉淀.该反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
分析 (1)根据常见仪器的名称、使用白色点滴板进行实验的优点,进行分析解答.
(2)根据碱溶液具有相似化学性质的原因,进行分析解答.
(3)根据碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,进行分析解答.
解答 解:(1)图中用于滴加指示剂的仪器的名称是胶头滴管.
使用点滴板进行实验,药品的用量少,则可节约药品,同时可减少对环境的污染,有时可以同时完成几个实验,便于观察比较.
(2)物质的结构决定物质的性质,氢氧化钙、氢氧化钠等碱类物质都能使指示剂变色,是因为不同的碱溶液中都含有相同的氢氧根离子,其离子符号为:OH-.
(3)碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,可观察到的现象是产生白色沉淀,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
故答案为:(1)胶头滴管;节约药品等;(2)OH-;(3)产生白色沉淀;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 本题难度不大,熟练掌握碱的化学性质、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
12.下列实验操作中,错误的是( )
| A. |  点燃酒精灯 | B. |  检查装置气密性 | C. |  加热液体 | D. |  蒸发食盐水 |
13.如图所示某原子的结构示意图,下列关于该原子的说法不正确的是( )
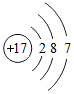

| A. | 它属于金属元素原子 | B. | 该原子有3个电子层 | ||
| C. | 该原子容易得到电子 | D. | 该原子最外层电子数为7 |
17.物质的结构决定性质,下列有关说法错误的是( )
| A. | 二氧化碳与一氧化碳化学性质不同的原因是分子构成不同 | |
| B. | 金刚石与石墨物理性质差异较大的原因是碳原子的结构不同 | |
| C. | 盐酸与硫酸化学性质相似的原因是在水溶液中都含有H+ | |
| D. | 氢氧化钠与氢氧化钙化学性质相似的原因是在水溶液中都含有OH- |
7.与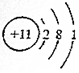 化学性质相似的是( )
化学性质相似的是( )
 化学性质相似的是( )
化学性质相似的是( )| A. | 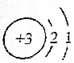 | B. |  | C. | 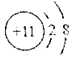 | D. | 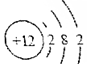 |
5. 人体缺碘会引起甲状腺肿大,幼儿缺碘影响生长发育,造成思维迟钝,结合图中信息判断,下列叙述中正确的是( )
人体缺碘会引起甲状腺肿大,幼儿缺碘影响生长发育,造成思维迟钝,结合图中信息判断,下列叙述中正确的是( )
 人体缺碘会引起甲状腺肿大,幼儿缺碘影响生长发育,造成思维迟钝,结合图中信息判断,下列叙述中正确的是( )
人体缺碘会引起甲状腺肿大,幼儿缺碘影响生长发育,造成思维迟钝,结合图中信息判断,下列叙述中正确的是( )| A. | 碘元素属于金属元素 | |
| B. | 碘原子的相对原子量是126.9g | |
| C. | 碘离子的核外电子数为54 | |
| D. | 碘原子在化学变化中易失去最外层电子 |
2.实验结束后,下列图示仪器处理正确的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
3.下列解释你认为合理的是( )
| A. | 汽油容易挥发,是因为汽油的分子容易变小 | |
| B. | 矿石可以被粉碎,是因为分子可以再分 | |
| C. | 电解水生成氢气和氧气,是因为原子的种类发生改变 | |
| D. | 10mL酒精与10mL水混合后体积小于20mL,是因为分子之间有间隔 |
 2017年,蚌埠到怀远要修建一条轻轨线,1号线起讫点为怀远老河湾和城南客运站,线程全程36.8公里,会大大方便人们的出行和和生活,如图是轻轨图.
2017年,蚌埠到怀远要修建一条轻轨线,1号线起讫点为怀远老河湾和城南客运站,线程全程36.8公里,会大大方便人们的出行和和生活,如图是轻轨图.