题目内容
7.与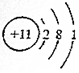 化学性质相似的是( )
化学性质相似的是( )| A. | 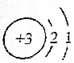 | B. |  | C. | 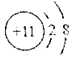 | D. | 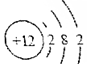 |
分析 元素的化学性质取决于该元素原子的最外层电子数,最外层电子数小于4,易失电子;最外层电子数大于4,易得电子;最外层电子数为8(He除外),性质稳定.
解答 解:由元素的化学性质跟它的原子的最外层电子数目有关,最外层电子数相同的元素化学性质相似, 的最外层电子数是1,选项中所给元素只有A的最外层电子数是1,故化学性质相似;
的最外层电子数是1,选项中所给元素只有A的最外层电子数是1,故化学性质相似;
故选A.
点评 在原子的结构示意图中,最外层电子数能反映出其化学性质,一般最外层电子数相同即具有相似的化学性质,但要注意与特殊的元素区别开来.

练习册系列答案
相关题目
17.工业上用氨气制取硝酸,发生如下反应:
①4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O
②2NO+O2═2NO2
③3NO2+H2O═2HNO3+NO
下列判断错误的是( )
①4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O
②2NO+O2═2NO2
③3NO2+H2O═2HNO3+NO
下列判断错误的是( )
| A. | NO的化学性质不稳定 | |
| B. | 反应①属于置换反应 | |
| C. | 尾气排放的NO、NO2会造成酸雨 | |
| D. | 制取硝酸过程中产生的NO可循环使用 |
15.下图所示的实验操作正确的是( )
| A. | 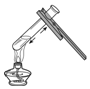 加热液体 | B. | 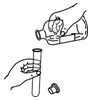 倾倒药品 | C. | 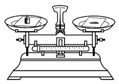 称量药品 | D. | 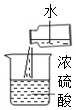 稀释浓硫酸 |
3.同学们,你们每年都过生日吗?生日蛋糕中的奶油常含有对人体有害的反式脂肪酸,其化学式为C18H34O2.下列说法正确的是( )
| A. | 反式脂肪酸是氧化物 | |
| B. | 反式脂肪酸由碳、氢、氧三种元素组成 | |
| C. | 反式脂肪酸由54个原子构成 | |
| D. | 反式脂肪酸中碳氧元素质量比是9:1 |
10.科学研究发现,乙醇(俗名酒精,化学式是C2H5OH)是重要的化工原料和燃料,但过量饮酒有害无益.
(1)乙醇属于有机物(填“无机物”或“有机物”).
(2)交警通常用一种“酒精检测仪”检查司机呼出气体中酒精的含量,其反应原理为:C2H5OH+4CrO3+6H2SO4═2Cr2(SO4)3+2X↑+9H2O,反应中红色的CrO3转变为绿色的Cr2(SO4)3,则X的化学式为CO2.
(3)汽车燃料所用的乙醇汽油是将乙醇与汽油按一定比例混合而成的一种燃料.
①乙醇属于A能源(填序号).
A.可再生 B.不可再生 C.化石
②在密闭容器中,将少量乙醇置于一定量氧气中燃烧,现测得反应前后各物质的质量如表:
如表中x的值为14,w一定是一氧化碳(写一种物质的名称).
(1)乙醇属于有机物(填“无机物”或“有机物”).
(2)交警通常用一种“酒精检测仪”检查司机呼出气体中酒精的含量,其反应原理为:C2H5OH+4CrO3+6H2SO4═2Cr2(SO4)3+2X↑+9H2O,反应中红色的CrO3转变为绿色的Cr2(SO4)3,则X的化学式为CO2.
(3)汽车燃料所用的乙醇汽油是将乙醇与汽油按一定比例混合而成的一种燃料.
①乙醇属于A能源(填序号).
A.可再生 B.不可再生 C.化石
②在密闭容器中,将少量乙醇置于一定量氧气中燃烧,现测得反应前后各物质的质量如表:
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水蒸汽 | w |
| 反应前质量/g | 23 | 40 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 22 | 27 | x |
7.下列说法正确的是( )
| A. | 20℃1L水与1L酒精混合后得到的混合溶液的体积恰好为2L | |
| B. | 20℃1g镁与1g稀硫酸充分反应后所得的溶液质量恰好为2g | |
| C. | 20℃1g氢氧化钠溶液中加入1g稀盐酸所得溶液质量恰好为2g | |
| D. | 20℃1g氯化钠饱和溶液中加1g氯化钠固体得到2g氯化钠溶液 |
8.下列实验,通过观察实验现象,不能达到实验目的是( )
| A. | 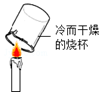 证明蜡烛中含有碳元素 | |
| B. | 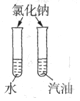 探究同种溶质在不同溶剂中的溶解性不同 | |
| C. | 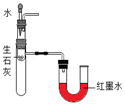 验证生石灰与水反应放热 | |
| D. | 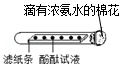 证明分子不断运动 |
 如图是实验室检验溶液的酸碱性的实验,请回答下列问题:
如图是实验室检验溶液的酸碱性的实验,请回答下列问题: