题目内容
根据下列化合物与单质相互转化的关系回答(反应条件已略去):

(1)若乙的溶液是浅绿色,Y是红色固体,则反应的化学方程式可能为 .
(2)若乙是空气中的成分,Y是红色固体,则X是 ,甲是 .(填化学式)

(1)若乙的溶液是浅绿色,Y是红色固体,则反应的化学方程式可能为
(2)若乙是空气中的成分,Y是红色固体,则X是
考点:物质的鉴别、推断,化学式的书写及意义,书写化学方程式、文字表达式、电离方程式
专题:常见物质的推断题
分析:(1)根据题目的信息可知:若化合物乙的溶液呈浅绿色,单质y是红色固体,浅绿色的溶液中含有亚铁离子,y是红色的单质,又是化合物和单质生成的,所以y就是铜,乙中含有亚铁离子,所以x就是铁;
(2)若乙是空气中的成分,可以是二氧化碳或水,单质Y是红色固体,可以是铜,根据常见的置换反应会进行分析.
(2)若乙是空气中的成分,可以是二氧化碳或水,单质Y是红色固体,可以是铜,根据常见的置换反应会进行分析.
解答:解:(1)若化合物乙的溶液呈浅绿色,单质y是红色固体,浅绿色的溶液中含有亚铁离子,y是红色的单质,又是化合物和单质生成的,所以y就是铜,乙中含有亚铁离子,所以x就是铁,因此可以是铁和硫酸铜反应产生硫酸亚铁和铜,故反应的方程式为:Fe+CuSO4═FeSO4+Cu(合理即可);
(2)若乙是空气中的成分,可以是二氧化碳或水,单质Y是红色固体,可以是铜,因此可以是碳和氧化铜或氢气和氧化铜的反应,故答案为:CO2(或H2);CuO.
(2)若乙是空气中的成分,可以是二氧化碳或水,单质Y是红色固体,可以是铜,因此可以是碳和氧化铜或氢气和氧化铜的反应,故答案为:CO2(或H2);CuO.
点评:此题主要是考查学生的综合分析能力,不但要求学生具备有关物质的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
相关题目
小明同学用排水集气法将气体充满集气瓶,然后把集气瓶口朝上放置在桌面上.这说明小明所收集的气体( )
| A、易溶于水,密度比空气小 |
| B、易溶于水,密度比空气大 |
| C、不易溶于水,密度比空气小 |
| D、不易溶于水,密度比空气大 |
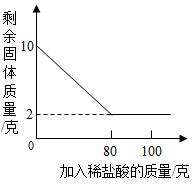 实验室常用石灰石和稀盐酸反应制取二氧化碳.某同学用质量为10克的石灰石和100克过量的稀盐酸反应,该同学测得的有关实验数据如图函数关系.(假定杂质不溶于水,也不参加反应)请回答下列问题:
实验室常用石灰石和稀盐酸反应制取二氧化碳.某同学用质量为10克的石灰石和100克过量的稀盐酸反应,该同学测得的有关实验数据如图函数关系.(假定杂质不溶于水,也不参加反应)请回答下列问题: