题目内容
为了测定某地石灰石中碳酸钙的质量分数,取7.5g样品放入烧杯,加入稀盐酸至不再产生气体,生成CO2气体的质量与滴加稀盐酸的质量关系如图所示(石灰石中的杂质均不溶于水且不与盐酸反应).(1)CO2的质量为______g.
(2)计算石灰石中碳酸钙的质量分数______.
(3)计算恰好完全反应后所得溶液中溶质的质量分数.
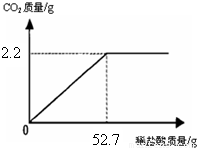
【答案】分析:(1)根据图象可判断最终生成二氧化碳的质量根据二氧化碳的质量可求出碳酸钙的质量;
(2)最后根据二氧化碳的质量可以求出反应的碳酸钙的质量,进而可求出石灰石中碳酸钙的质量分数;
(2)据图可看出石灰石样品恰好完全反应时所加稀盐酸的质量为52.7g,所得溶液的质量=所加入的所有物质的质量总和-生成气体的质量-杂质的质量,而溶液中的溶质氯化钙则可由化学方程式中二氧化碳质量可以求出;
解答:解:(1)由图象可知反应后生成的二氧化碳的质量是2.2g.
(2)设碳酸钙的质量为x,生成的氯化钙的质量为y,
则CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 111 44
x y 2.2g
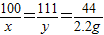 ,
,
解得x=5g,y=5.55g,
该样品中碳酸钙的质量分数为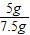 ×100%=66.7%,
×100%=66.7%,
(3)因杂质既不溶于水,也不与其他物质反应,则溶液的质量为7.5g+52.7g-(7.5g-5g)-2.2g=55.5g,溶质的质量为11.1g,则溶质的质量分数为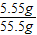 ×100%=10%,
×100%=10%,
故答案为:(1)2.2g;(2)66.7%;(3)答:反应后所得溶液中溶质的质量分数为10%.
点评:求反应后所得溶液的质量的计算是初中化学计算的一个重点内容,其方法一般是:所加入的所有物质的质量总和-生成气体的质量或生成沉淀的质量.
(2)最后根据二氧化碳的质量可以求出反应的碳酸钙的质量,进而可求出石灰石中碳酸钙的质量分数;
(2)据图可看出石灰石样品恰好完全反应时所加稀盐酸的质量为52.7g,所得溶液的质量=所加入的所有物质的质量总和-生成气体的质量-杂质的质量,而溶液中的溶质氯化钙则可由化学方程式中二氧化碳质量可以求出;
解答:解:(1)由图象可知反应后生成的二氧化碳的质量是2.2g.
(2)设碳酸钙的质量为x,生成的氯化钙的质量为y,
则CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 111 44
x y 2.2g
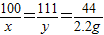 ,
,解得x=5g,y=5.55g,
该样品中碳酸钙的质量分数为
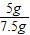 ×100%=66.7%,
×100%=66.7%,(3)因杂质既不溶于水,也不与其他物质反应,则溶液的质量为7.5g+52.7g-(7.5g-5g)-2.2g=55.5g,溶质的质量为11.1g,则溶质的质量分数为
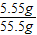 ×100%=10%,
×100%=10%,故答案为:(1)2.2g;(2)66.7%;(3)答:反应后所得溶液中溶质的质量分数为10%.
点评:求反应后所得溶液的质量的计算是初中化学计算的一个重点内容,其方法一般是:所加入的所有物质的质量总和-生成气体的质量或生成沉淀的质量.

练习册系列答案
相关题目
为了测定某地石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行如下实验:(请写出详细的计算过程)
(1)碳酸钙的相对分子质量是 ,碳酸钙的组成中一共有 种非金属元素.
(2)计算这种石灰石样品中碳酸钙的质量分数.
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量(g) | 5 | 10 | 15 | 20 |
| 生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | 4.4 |
(2)计算这种石灰石样品中碳酸钙的质量分数.