题目内容
下列分析合理的是( )
| A、向某溶液中滴加AgNO3溶液,产生白色沉淀,则该溶液一定含有稀盐酸 |
| B、FeCl3、Na2SO4、KCl、Ba(OH)2四种溶液,不用其它试剂一定可将它们鉴别开来 |
| C、某无色溶液中通入CO2气体有白色沉淀生成,则该无色溶液中一定含有Ca2+ |
| D、某固体中滴入稀盐酸产生能使澄清石灰水变浑浊的气体,则该固体中一定含有碳酸盐 |
考点:酸的化学性质,酸、碱、盐的鉴别
专题:物质的鉴别题,常见的酸 酸的通性
分析:A、考虑氯离子和银离子结合生成氯化银白色沉淀;
B、先利用颜色鉴别出FeCl3、再利用FeCl3、Ba(OH)2溶液生成红褐色沉淀;Na2SO4、Ba(OH)2溶液产生白色沉淀;
C、考虑碳酸钡、碳酸钙、碳酸锌、碳酸银等都为白色沉淀;
D、考虑碳酸氢盐也能与稀盐酸产生能使澄清石灰水变浑浊的气体.
B、先利用颜色鉴别出FeCl3、再利用FeCl3、Ba(OH)2溶液生成红褐色沉淀;Na2SO4、Ba(OH)2溶液产生白色沉淀;
C、考虑碳酸钡、碳酸钙、碳酸锌、碳酸银等都为白色沉淀;
D、考虑碳酸氢盐也能与稀盐酸产生能使澄清石灰水变浑浊的气体.
解答:解:
A、只要溶液中含有氯离子,向其中滴加AgNO3溶液,就产生白色沉淀,故原说法错误;
B、因为FeCl3为黄色溶液,则可先利用颜色鉴别出FeCl3、再根据铁离子与氢氧根离子生成红褐色沉淀、硫酸根离子与钡离子产生白色沉淀,可以鉴别出Ba(OH)2、Na2SO4,则剩余的为KCl;故分析正确;
C、某无色溶液中通入CO2气体有白色沉淀生成,则该无色溶液中,可能含有钡离子、银离子钙离子等,故原说法错误;
D、某固体中滴入稀盐酸产生能使澄清石灰水变浑浊的气体,则该固体中可能含有碳酸盐、碳酸氢盐.故原说法错误.
故选:B.
A、只要溶液中含有氯离子,向其中滴加AgNO3溶液,就产生白色沉淀,故原说法错误;
B、因为FeCl3为黄色溶液,则可先利用颜色鉴别出FeCl3、再根据铁离子与氢氧根离子生成红褐色沉淀、硫酸根离子与钡离子产生白色沉淀,可以鉴别出Ba(OH)2、Na2SO4,则剩余的为KCl;故分析正确;
C、某无色溶液中通入CO2气体有白色沉淀生成,则该无色溶液中,可能含有钡离子、银离子钙离子等,故原说法错误;
D、某固体中滴入稀盐酸产生能使澄清石灰水变浑浊的气体,则该固体中可能含有碳酸盐、碳酸氢盐.故原说法错误.
故选:B.
点评:本题考查了常见物质的鉴别,完成此题,可以依据已有的知识结合物质的性质进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
法医常用“马氏试砷法”来检验动物是否砒霜(R)中毒,其化学原理为:R+8HCl+4Zn═4ZnCl2+3H2O+2As+H2↑,则砒霜的化学式为( )
| A、As2O2 |
| B、As2O |
| C、AsO |
| D、As2O3 |
核能是人类历史上的一项伟大发现,核能发电不会造成空气污染,使用的燃料体积小,运输和储存都很方便,氘和氚都是未来产生核能的燃料,它们都是氢元素的一种原子,则氘原子和氚原子的质子数分别是( )
| A、2和3 | B、1和3 |
| C、1和1 | D、1和2 |
用pH试纸测定溶液的酸碱度的方法中正确的是( )
| A、将试纸伸入待测液中 |
| B、将试纸用水润湿后放在玻璃片上,用玻璃棒蘸取溶液滴在试纸上 |
| C、将待测液倒入玻璃片上的试纸上 |
| D、把试纸放在玻璃片上,用玻璃棒蘸取溶液滴在试纸上 |
下列溶液中分别放入锌粒,一段时间后取出,溶液质量减少的是( )
| A、MgCl2 溶液 |
| B、稀盐酸 |
| C、硫酸亚铁溶液 |
| D、AgNO3溶液 |
 据报道,我国“蛟龙”号载人潜水器于2012年6月27日成功下潜至7 062米深度,再创世界纪录.下列反应都能产生氧气,其中最适宜在潜水器里供给氧气的反应是( )
据报道,我国“蛟龙”号载人潜水器于2012年6月27日成功下潜至7 062米深度,再创世界纪录.下列反应都能产生氧气,其中最适宜在潜水器里供给氧气的反应是( )A、2KMnO4
| ||||
B、2H2O
| ||||
| C、2Na2O2+2CO2═2Na2CO3+O2 | ||||
D、2H2O2
|
为探究Fe、Cu、Ag 三种金属的活动性顺序,某兴趣小组设计了如图所示的四组实验方案,你认为不可行的是( )
A、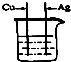 FeSO4溶液 |
B、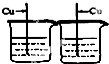 FeSO4溶液 AgNO3溶液 |
C、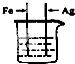 CuSO4溶液 |
D、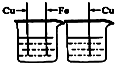 稀盐酸 AgNO3溶液 |
 如图是小华同学用高锰酸钾制取氧气的实验装置图.
如图是小华同学用高锰酸钾制取氧气的实验装置图.