题目内容
7.化学兴趣小组欲用石灰石(杂质不与盐酸反应也不溶于水)测定某盐酸的溶质质量分数,他们设计了如图所示的实验.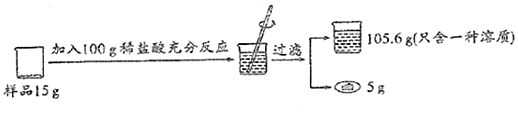
请完成下列分析及计算:
(1)反应生成的二氧化碳的质量为4.4g.
(2)计算该稀盐酸的溶质质量分数.
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算HCl的质量,进而求算对应的质量分数
解答 解:根据质量守恒定律,二氧化碳的质量为:100g+15g-105.6g-5g=4.4g;
设稀盐酸中溶质的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
x 4.4g
$\frac{73}{44}$=$\frac{x}{4.4g}$
x=7.3g
该稀盐酸的溶质质量分数为$\frac{7.3g}{100g}$×100%=7.3%
答:(1)反应生成的二氧化碳的质量为 4.4g.
(2)该稀盐酸的溶质质量分数为7.3%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
17.下列符号中既表示一种元素,又表示一个原子,还能表示一种单质的是( )
| A. | O | B. | O2 | C. | 2O2 | D. | Fe |
18.有利于保护环境的是( )
| A. |  随意扔垃圾 | B. |  废水排入河流 | ||
| C. |  金属回收再利用 | D. |  废气排到高空 |
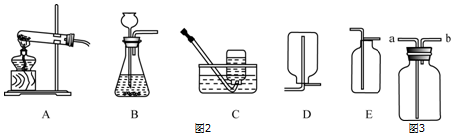
15.广口瓶在化学实验中有许多用途:
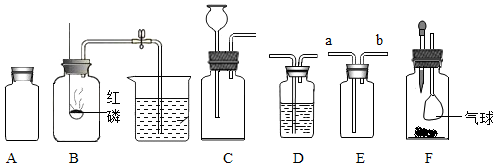
(1)A仪器可用来盛放固态的药品(填“固、液、气”);
(2)B实验的目的是测定空气中氧气的含量;
(3)用C装置制取氧气的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)用D装置除去CO中混有的CO2,D装置中应装的药品是氢氧化钠(或氢氧化钙等)溶液;
(5)用排气法收集氧气,氧气应从E装置的a端通入;
(6)用F装置进行实验,下列A组药品,可使气球膨胀.

(1)A仪器可用来盛放固态的药品(填“固、液、气”);
(2)B实验的目的是测定空气中氧气的含量;
(3)用C装置制取氧气的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)用D装置除去CO中混有的CO2,D装置中应装的药品是氢氧化钠(或氢氧化钙等)溶液;
(5)用排气法收集氧气,氧气应从E装置的a端通入;
(6)用F装置进行实验,下列A组药品,可使气球膨胀.
| A组 | B组 | C组 | |
| 固体 | 硝酸铵 | 碳酸钙 | 氢氧化钠 |
| 液体 | 水 | 稀盐酸 | 水 |
2.下列选项中的描述与图象不相符的是( )
| A. | 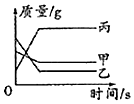 由密闭容器中三种物质的质量变化推测该反应的化合反应 | |
| B. |  将水通电一段时间后,水分解生成的气体质量随时间的变化 | |
| C. | 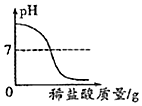 向一定量的氢氧化钠溶液中滴加稀盐酸,溶液pH的变化 | |
| D. | 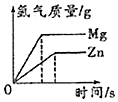 等质量的镁粉与锌粉分别和过量的等浓度稀盐酸反应 |
12.下列基本实验操作不正确的是( )
| A. |  用胶头滴管取液体 | B. |  读取液体体积 | ||
| C. |  稀释浓硫酸 | D. |  闻气体的气味 |
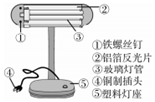 青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.
青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具.