题目内容
17.如图中①~③是固体甲在一定量水中进行的溶解实验.
(1)图中④可表示固体甲的溶解度曲线的是B(选填“A”或“B”);
(2)①、②、③所示溶液一定是饱和溶液的是②;
(3)若A中混有少量的B,提纯A的方法是降温结晶;
(4)35℃时,将等质量的A和B配成饱和溶液(A、B均不与水反应,且不考虑溶解时的温度变化),需要水的质量关系是B>A.
分析 根据物质的溶解过程可以判断物质的溶解度曲线;
饱和溶液和不饱和溶液之间可以相互转化;
从溶液中结晶的方法有两种:蒸发结晶和降温结晶,物质的溶解度受温度变化影响较小时,应该用蒸发结晶;物质的溶解度受温度变化影响较大时,应该用降温结晶.
解答 解:(1)图中①~③变化过程中,降低温度时固体能够继续溶解,说明甲的溶解度随着温度升高而减小,因此图中④可表示固体甲的溶解度曲线的是B.
故填:B.
(2)①、②、③中,②中含有不溶于水的固体,说明一定是饱和溶液.
故填:②.
(3)A的溶解度随着温度升高而增大,B的溶解度随着温度升高而减小,因此若A中混有少量的B,可以通过降温结晶提纯A.
故填:降温结晶.
(4)35℃时,A的溶解度大于B的溶解度,将等质量的A和B配成饱和溶液,需要水的质量关系是B>A.
故填:B>A.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8. 甲、乙是两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙是两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙是两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙是两种固体物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲的溶解度比乙大 | |
| B. | t1℃时,甲的饱和溶液中溶质与溶液的质量比为1:5 | |
| C. | t2℃时,甲、乙两物质饱和溶液溶质的质量分数相等 | |
| D. | t3℃时,将甲、乙两物质的饱和溶液分别降温至t2℃,析出晶体的质量为甲>乙 |
 图A为镁原子的结构示意图,图B是镁元素在元素周期表中的部分信息,据此回答下列问题.
图A为镁原子的结构示意图,图B是镁元素在元素周期表中的部分信息,据此回答下列问题.
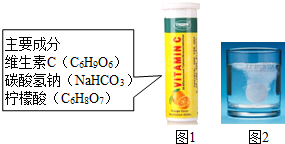 某研究小组发现,维C泡腾片(主要成分如图所示)溶于水,有许多气泡产生,小组同学对该气体的成分进行了如下探究:
某研究小组发现,维C泡腾片(主要成分如图所示)溶于水,有许多气泡产生,小组同学对该气体的成分进行了如下探究: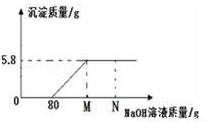
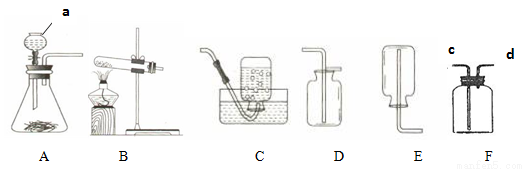
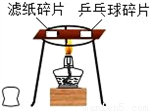
 5nH2O + _________________。
5nH2O + _________________。