题目内容
2. 眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图:
眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图:(1)所标物质中属于金属单质的是铜,属于有机合成材料的塑料.
(2)夏天铜螺丝部位常出现一层绿色物质,这是由于铜生锈的原因,防止铜螺丝生锈你的方法是清洗并抹干净或涂油.
(3)该款变色眼镜的玻璃里加入了溴化银(AgBr)和氧化铜.在强光照射下,溴化银分解成溴(Br2)和银,玻璃颜色变深;当光线变暗时,溴和银在氧化铜作用下,重新生成溴化银,玻璃颜色变浅.请写出上述过程中的一条化学方程式2AgBr$\frac{\underline{\;强光\;}}{\;}$ 2Ag+Br2.
(4)结合镜片材料从天然水晶、光学玻璃到光学树脂的变迁过程,请你谈一谈化学与生活的关系:化学在保障人类生存和提高人类生活质量方面有重要作用.
分析 (1)根据材料的分类知识进行分析;
(2)根据防锈的措施进行分析;
(3)根据题意,溴化银受强光照射时会分解为银和溴Br2,当光线变暗(弱)时,银和溴在催化剂氧化铜的作用下,又重新化合生成溴化银,写出反应的化学方程式即可;
(4)可从化学材料的开发意义分析解答.
解答 解:(1)铜螺丝属于金属单质,塑料脚套属于有机合成材料,故填:铜螺丝,塑料脚套;
(2)铜生锈是铜与空气中的水和二氧化碳起作用,故防止铜螺丝生锈你的方法是 清洗并抹干净或涂油.
(3)溴化银受强光照射时会分解为银和溴Br2,2AgBr$\frac{\underline{\;强光\;}}{\;}$2Ag+Br2;当光线变暗(弱)时,银和溴在催化剂氧化铜的作用下,又重新化合生成溴化银,2Ag+Br2 $\frac{\underline{\;CuO\;}}{\;}$2AgBr;
(4)从镜片材料从天然水晶、光学玻璃到光学树脂的变迁过程可以看出化学在材料的开发和利用中发挥着重要作用.
故答案为:(1)铜;塑料;
(2)清洗并抹干净或涂油等等;
(3)2AgBr$\frac{\underline{\;强光\;}}{\;}$2Ag+Br2( 或“2Ag+Br2 $\frac{\underline{\;CuO\;}}{\;}$2AgBr”);
(4)化学在保障人类生存和提高人类生活质量方面有重要作用(或生活离不开化学).
点评 本题难度不大,利用化学反应前后元素守恒、原子守恒来确定物质的化学式以及掌握物质的分类等是正确解题的关键.

练习册系列答案
相关题目
13.为研究铝和铜的金属活动性,某研究小组进行如下探究.
(1)小明设计的实验方案是:将打磨的铝片和铜片分别放入稀盐酸中,观察反应的现象.写出铝与盐酸反应的化学方程式2Al+6HCl=2AlCl3+3H2↑.
(2)小芳将铝片放入氯化铜溶液中,看到有大量气泡逸出,且在一段时间内产生气泡越来越快,收集该气体可点燃,则生成的气体可能是氢气(或“H2”).
(3)小芳在(2)实验中,还观察到铝片与浓氯化铜溶液反应时还有“白色沉淀”这一异常现象.
【提出问题】铝片与浓氯化铜溶液反应反应出现的白色沉淀的组成是什么?
【查阅文献】①AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
②CuCl为白色固体,不溶于水、乙醇;溶于浓盐酸且溶液变蓝色.
【提出合理假设】
假设a:该白色沉淀可能含有CuCl(或者“CuCl”和“AlCl3”);
假设b:该白色沉淀可能含有AlCl3;
假设c:该白色沉淀可能含有Al.
【设计并完成实验】取白色沉淀分别进行如下实验:
【得出结论】实验①可判断假设c不成立(填“成立”或“不成立”),再结合实验②和③可得出该白色沉淀的成分是CuCl和AlCl3.
(4)室温时,小芳将等质量的相同铝片分别放入氯化铜溶液和硫酸铜溶液中,发现铝片和氯化铜溶液反应剧烈.
【发现问题】为什么铝片与氯化铜溶液反应比与硫酸铜溶液反应更剧烈呢?
【提出假设】①Cl-使铜盐和铝的反应容易进行.②氯化铜溶液和硫酸铜溶液的浓度不同所致.
【设计实验】为验证假设①是否正确,请设计一个合理的实验:取打磨的铝片放在一定体积的硫酸铜溶液中,滴加氯化钠溶液.
(1)小明设计的实验方案是:将打磨的铝片和铜片分别放入稀盐酸中,观察反应的现象.写出铝与盐酸反应的化学方程式2Al+6HCl=2AlCl3+3H2↑.
(2)小芳将铝片放入氯化铜溶液中,看到有大量气泡逸出,且在一段时间内产生气泡越来越快,收集该气体可点燃,则生成的气体可能是氢气(或“H2”).
(3)小芳在(2)实验中,还观察到铝片与浓氯化铜溶液反应时还有“白色沉淀”这一异常现象.
【提出问题】铝片与浓氯化铜溶液反应反应出现的白色沉淀的组成是什么?
【查阅文献】①AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
②CuCl为白色固体,不溶于水、乙醇;溶于浓盐酸且溶液变蓝色.
【提出合理假设】
假设a:该白色沉淀可能含有CuCl(或者“CuCl”和“AlCl3”);
假设b:该白色沉淀可能含有AlCl3;
假设c:该白色沉淀可能含有Al.
【设计并完成实验】取白色沉淀分别进行如下实验:
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量浓盐酸 | 无气泡,固体溶解,得到褐色溶液 |
| ② | 加入适量无水乙醇 | 固体部分溶解 |
| ③ | 加入适量浓氨水 | 固体部分溶解,得到蓝色溶液 |
(4)室温时,小芳将等质量的相同铝片分别放入氯化铜溶液和硫酸铜溶液中,发现铝片和氯化铜溶液反应剧烈.
【发现问题】为什么铝片与氯化铜溶液反应比与硫酸铜溶液反应更剧烈呢?
【提出假设】①Cl-使铜盐和铝的反应容易进行.②氯化铜溶液和硫酸铜溶液的浓度不同所致.
【设计实验】为验证假设①是否正确,请设计一个合理的实验:取打磨的铝片放在一定体积的硫酸铜溶液中,滴加氯化钠溶液.
10.将下列各组中物质放入烧杯中,加适量水搅拌,待充分反应后过滤,在滤纸上留下两种金属的是( )
| A. | Fe(过量)、KNO3、CuSO4 | B. | Fe(过量)、Cu(NO3)2、AgNO3 | ||
| C. | Zn、NaCl、CuCl2(过量) | D. | Cu(过量)、FeCl2、HCl |
7.下列各组物质的溶液不用其它试剂就可鉴别的是( )
| A. | CaCl2、K2CO3、HCl、(NH4)2CO3 | B. | HCl、CuSO4、KNO3、Na2SO4 | ||
| C. | FeCl3、HCl、NaCl、NaOH | D. | Na2CO3、Na2SO4、HCl、H2SO4 |
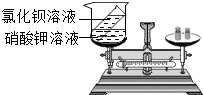 小贝设计如图所示的实验来验证质量守恒定律.将图示中的两种溶液混合前后天平仍然平衡,小贝认为实验成功,你认为小贝的实验设计合理吗?为什么?
小贝设计如图所示的实验来验证质量守恒定律.将图示中的两种溶液混合前后天平仍然平衡,小贝认为实验成功,你认为小贝的实验设计合理吗?为什么? 通过化学启蒙学习,同学们对组成万物的基本物质有了进一步的了解.
通过化学启蒙学习,同学们对组成万物的基本物质有了进一步的了解.