题目内容
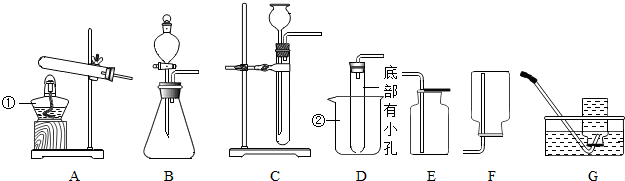
1.根据如图所示要求回答问题:
(1)图中仪器a的名称是锥形瓶,b的名称是水槽,从A装置设计来看,该反应需要的反应条件是加热.
(2)实验室可用B装置制取二氧化碳,反应的原料为大理石或石灰石和稀盐酸(填名称).
(3)若用C装置收集氧气,发现收集到的氧气不纯,可能原因是集气瓶收集气体前没有装满水(或刚有气泡冒出就开始收集气体).
(4)下列几种气体可用D装置干燥、收集的是①⑤⑥(填序号).
①H2 ②O2 ③CO2 ④SO2 ⑤CH4 ⑥NH3.
分析 (1)熟记仪器名称和装置的特点;
(2)根据实验室中制取二氧化碳的原料来分析;
(3)据排水法收集氧气的注意事项分析解答;
(4)由图示可知气体用碱石灰来干燥,说明气体是显中性或碱性,不能是酸性气体,由收集方法可知该气体密度比空气小.
解答 解:(1)a是锥形瓶,b是水槽,根据装置A中有酒精灯,所以反应条件是加热;故填:锥形瓶;水槽;加热;
(2)在实验室里,常用大理石或石灰石和稀盐酸反应来制取二氧化碳.故填:大理石或石灰石和稀盐酸;
(3)利用排水法收集时的氧气不纯,可能是集气瓶内未装满水,留有气泡,也有可能是收集时未等气泡连续、均匀冒出据开始收集,从而导致收集的气体中混有空气;故填:集气瓶收集气体前没有装满水(或刚有气泡冒出就开始收集气体);
(4)H2属于中性气体,且密度比空气小,符合要求;O2密度比空气大,不符合要求;CO2密度比空气大,且属于酸性气体不符合要求;SO2属于酸性气体,且密度比空气大,不符合要求;CH4密度比空气小,且属于中性气体,符合要求;NH3密度比空气小,属于碱性气体,符合题意.
故选:①⑤⑥.
点评 碱性气体只能用来干燥中性气体或碱性气体,用排空气法收集气体时,主要考虑密度比空气大还是小.

练习册系列答案
相关题目
12. 和
和 分别表示质子数不同的两种原子,下列能表示混合物的是( )
分别表示质子数不同的两种原子,下列能表示混合物的是( )
 和
和 分别表示质子数不同的两种原子,下列能表示混合物的是( )
分别表示质子数不同的两种原子,下列能表示混合物的是( )| A. |  | B. |  | C. |  | D. |  |
16.铁在生产生活中应用十分广泛.铁的冶炼和利用已成为目前科学研究和技术领域中的重要课题.
一、生活中使用的防寒热贴利用了铁生锈原理,其工作过程中实现了由化学能转化为热能.
二、铁矿石冶炼成铁是一个复杂的过程,把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭和氧气反应生成的一氧化碳把铁从铁矿石里还原出来,得到铁合金.一氧化碳还原氧化铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(1)甲同学为探究铁合金中铁的质量分数,先后进行了四次实验(杂质不与稀硫酸反应),实验数据如下表:
请回答:上表第四次实验中合金里的铁恰好与稀硫酸完全反应,则Y=0.9g,该铁合金中铁的质量分数是多少?(写出计算过程)?84%
(2)乙同学提出单质碳也具有还原性,碳还原氧化铁的化学方程式为2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑,为什么工业上不用焦炭作为还原剂直接还原铁矿石?于是,他模拟工业炼铁设计如下对比实验(查阅资料知NaOH溶液可吸收CO2气体):
①取两份相同质量的氧化铁粉末.一份与足量的碳粉均匀混合放入下图装置A的硬质试管中;另一份放入下图装置B的硬质玻璃管中.
②装置A和B两组实验同时开始进行.在装置B的发应中,实验开始前,先通CO(选填“通CO”或“加热”);实验结束后,继续通入CO直至冷却至室温.

此时,发现装置B的硬质玻璃管中固体完全由红色变为黑色,装置A的硬质试管中仍有红色固体.因而他认为焦炭和铁矿石都是固体,接触面积小,不易完全反应是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因.
(3)丙同学经过查阅资料发现除了上述原因外,工业上不用焦炭作为还原剂直接还原铁矿石还有一些其它原因,试写出其中的一个生铁和焦炭都是固体,不易分离.
(4)丁同学利用图B装置,取不同质量的铁的氧化物进行实验.所得实验数据如下:
从上表可以看出进行第2次实验时,所得数据十分不可靠.请分析造成此种结果的原因主要可能是反应时间太短.
一、生活中使用的防寒热贴利用了铁生锈原理,其工作过程中实现了由化学能转化为热能.
二、铁矿石冶炼成铁是一个复杂的过程,把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭和氧气反应生成的一氧化碳把铁从铁矿石里还原出来,得到铁合金.一氧化碳还原氧化铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(1)甲同学为探究铁合金中铁的质量分数,先后进行了四次实验(杂质不与稀硫酸反应),实验数据如下表:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 所取合金的质量∕g | 10 | 10 | 20 | 30 |
| 所加稀硫酸的质量∕g | 100 | 120 | 80 | X |
| 生成氢气的质量∕g | 0.3 | 0.3 | 0.3 | Y |
(2)乙同学提出单质碳也具有还原性,碳还原氧化铁的化学方程式为2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑,为什么工业上不用焦炭作为还原剂直接还原铁矿石?于是,他模拟工业炼铁设计如下对比实验(查阅资料知NaOH溶液可吸收CO2气体):
①取两份相同质量的氧化铁粉末.一份与足量的碳粉均匀混合放入下图装置A的硬质试管中;另一份放入下图装置B的硬质玻璃管中.
②装置A和B两组实验同时开始进行.在装置B的发应中,实验开始前,先通CO(选填“通CO”或“加热”);实验结束后,继续通入CO直至冷却至室温.

此时,发现装置B的硬质玻璃管中固体完全由红色变为黑色,装置A的硬质试管中仍有红色固体.因而他认为焦炭和铁矿石都是固体,接触面积小,不易完全反应是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因.
(3)丙同学经过查阅资料发现除了上述原因外,工业上不用焦炭作为还原剂直接还原铁矿石还有一些其它原因,试写出其中的一个生铁和焦炭都是固体,不易分离.
(4)丁同学利用图B装置,取不同质量的铁的氧化物进行实验.所得实验数据如下:
| 实验序号 | 铁的氧化物质量/g | 生成铁的质量/g |
| 1 | 4.00 | 2.81 |
| 2 | 8.00 | 7.62 |
| 3 | 10.00 | 7.01 |
| 4 | 12.00 | 8.42 |
| 5 | 14.00 | 9.81 |
| 6 | 16.00 | 11.22 |
| 7 | 18.00 | 12.63 |
| 8 | 20.00 | 14.03 |
6.下列不属于化学研究范畴的是( )
| A. | 纳米铜的性质 | B. | 空气的组成 | C. | 单晶硅的结构 | D. | 电脑程序的研发 |
 某化学实验小组在实验室中对一烧杯浑浊的河水进行了简单净化.如图是过滤操作的装置图,请回答下列有关问题:
某化学实验小组在实验室中对一烧杯浑浊的河水进行了简单净化.如图是过滤操作的装置图,请回答下列有关问题: 黄铜(铜锌合金)是重要的金属材料,为研究某黄铜样品的组成,称取黄铜样品10g,往样品中加入稀硫酸,实验情况如图所示.
黄铜(铜锌合金)是重要的金属材料,为研究某黄铜样品的组成,称取黄铜样品10g,往样品中加入稀硫酸,实验情况如图所示.