题目内容
17.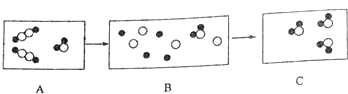 如图用●代表氢原子,〇代表氧子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如下:
如图用●代表氢原子,〇代表氧子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如下:(1)在C图中将相关粒子的图形补充完整.
(2)此变化前后没发生改变的微观粒子有氢原子、氧原子、水分子.
(3)A到B的过程的微观实质是在一定条件下,过氧化氢分子分解成氢原子和氧原子..
分析 (1)根据质量守恒定律将C图中将相关粒子的图形补充完整;
(2)根据微粒的变化分析此变化前后没发生改变的微观粒子;
(3)根据微粒的变化分析A到B的过程的微观实质;
解答 解:(1)由质量守恒定律反应前后原子的种类及数目不变可知,在C图中应补充一个 ;
;
(2)由微粒的变化可知,此变化前后没发生改变的微观粒子有:氢原子、氧原子、水分子;
(3)由微粒的变化可知,A到B的过程的微观实质是:在一定条件下,过氧化氢分子分解成氢原子和氧原子.
故答为:(1)补 ;(2)氢原子、氧原子、水分子;(3)在一定条件下,过氧化氢分子分解成氢原子和氧原子.
;(2)氢原子、氧原子、水分子;(3)在一定条件下,过氧化氢分子分解成氢原子和氧原子.
点评 本题主要考查了反应前后的物质种类及其原子种类等方面的关系问题,解题的关键是依据质量守恒以及对图示微粒的认识.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
8.下列叙述,你认为科学的是( )
| A. | 洗涤剂去除油污是因为洗涤剂可以溶解油污 | |
| B. | 钢丝球洗刷铝制炊具 | |
| C. | 霉变大米加热后可食用 | |
| D. | 减少使用塑料制品可以减少白色污染 |
5.废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如图所示:

(1)在反应器中发生反应的化学方程式除 Fe2(SO4)3+Fe=3FeSO4外,还有Fe+H2SO4═FeSO4+H2↑;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(2)滤液 M 中肯定含有的溶质的离子是Fe2+、H+、SO42-(填离子符号).
(3)在实验室中完成操作 A 的名称是过滤.
(4)滤液 M 经过操作 B 可得硫酸亚铁晶体(FeSO4•7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如下表:
根据溶解度表,硫酸亚铁晶体(FeSO4•7H2O)冷却结晶温度最高不超过60℃.

(1)在反应器中发生反应的化学方程式除 Fe2(SO4)3+Fe=3FeSO4外,还有Fe+H2SO4═FeSO4+H2↑;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(2)滤液 M 中肯定含有的溶质的离子是Fe2+、H+、SO42-(填离子符号).
(3)在实验室中完成操作 A 的名称是过滤.
(4)滤液 M 经过操作 B 可得硫酸亚铁晶体(FeSO4•7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | ||
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||||
12.对下列相关事实用微观粒子的知识解释正确的是( )
| 选项 | 事 实 | 解释 |
| A | 氯化钠固体不导电 | 氯化钠固体中没有离子 |
| B | 有机物数目种类异常庞大 | 原子的排列方式不同,性质不同 |
| C | 水烧开后水壶盖容易被顶起 | 温度升高分子运动加快,体积变大 |
| D | 水结冰后不能流动 | 0℃以下,水分子不再运动 |
| A. | A | B. | B | C. | C | D. | D |
6.蔗糖(C12H22O11)在甜菜、甘蔗中含量极高.下列有关C12H22O11的说法正确的是( )
| A. | C12H22O11属于氧化物 | |
| B. | 一个蔗糖分子中碳原子的质量为144g | |
| C. | C12H22O11中氢元素的质量分数最大 | |
| D. | C12H22O11中氢、氧原子的个数比为2:1 |
7.维生素C(化学式为C6H8O6)是人体不可缺少的营养物质.下列关于维生素C的叙述正确的是( )
| A. | 是氧化物 | |
| B. | 氧元素的质量分数计算式为$\frac{6}{176}$×100% | |
| C. | 每个分子中含有20个原子 | |
| D. | 碳、氢、氧三种元素的质量比3:4:3 |
