题目内容
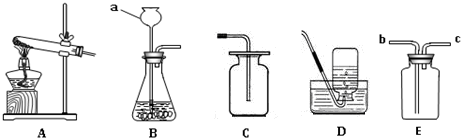
2.小明同学发现家里有一瓶无标签的无色液体A,她为了探究它是何种物质,做了如下实验:在A中加入一种黑色粉末B,稍微振荡,在常温下就能迅速产生气体C并收集了一瓶该气体,且黑色粉末B的质量在反应前后没有改变.她又取一种淡黄色粉末D点燃放入C中,产生明亮的蓝紫色火焰,生成一种有刺激性气味的气体E.(1)、写出下列各物质的化学式:AH2O2、BMnO2、CO2、ESO2
(2)、写出上述有关的反应(用化学式表达),并在后面的括号内注明其基本反应类型:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(分解反应);S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2(化合反应).
分析 根据取一种淡黄色粉末D点燃放入C中,产生明亮的蓝紫色火焰,生成一种有刺激性气味的气体E,所以C有助燃性,C是氧气,D是硫,硫和氧气反应生成二氧化硫,所以E是二氧化硫,在A中加入一种黑色粉末B,稍微振荡,在常温下就能迅速产生氧气,且黑色粉末B的质量在反应前后没有改变,所以A是过氧化氢溶液,B是二氧化锰,然后将推出的物质进行验证即可.
解答 解:(1)取一种淡黄色粉末D点燃放入C中,产生明亮的蓝紫色火焰,生成一种有刺激性气味的气体E,所以C有助燃性,C是氧气,D是硫,硫和氧气反应生成二氧化硫,所以E是二氧化硫,在A中加入一种黑色粉末B,稍微振荡,在常温下就能迅速产生氧气,且黑色粉末B的质量在反应前后没有改变,所以A是过氧化氢溶液,B是二氧化锰,经过验证,推导正确,所以A是H2O2,B是MnO2,C是O2,E是SO2;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应满足分解反应一变多的条件,属于分解反应;
硫和氧气在点燃的条件下生成二氧化硫,化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,该反应满足化合反应多变一的条件,属于化合反应.
故答案为:(1)H2O2,MnO2,O2,SO2;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,分解反应;
S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,化合反应.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | 在原子钟,核电荷数一定等于质子数或核外电子数 | |
| B. | 原子核都是有质子和中子构成 | |
| C. | 原子核带正电 | |
| D. | 原子核体积很小但质量却很大,核外电子围绕着原子核作高速运动 |
| A. | 由两种物质生成一种物质的反应叫做化合反应 | |
| B. | 氧化反应是指物质与氧气发生的化合反应 | |
| C. | 蜡烛的燃烧过程既有物理变化,又有化学变化 | |
| D. | 凡是在空气中不能燃烧的物质,在纯氧中也不能燃烧 |
| A. | 2g的氢气和8g的氧气充分反应生成10g的水 | |
| B. | 水结成冰的前后总质量不发生改变,这有力地证明了质量守恒定律 | |
| C. | 铁丝在氧气燃烧后增加的质量等于参加反应的氧气的质量 | |
| D. | 100克高锰酸钾完全分解所得固体的质量为100克 |

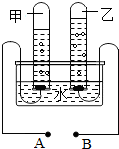 北京时间1月13日05:53海地发生的7.0级强震已给海地造成严重灾难,一名外国救援人员直言:“现在金钱就如粪土,水才是货币”.下列是关于水的研究,请回答有关问题:
北京时间1月13日05:53海地发生的7.0级强震已给海地造成严重灾难,一名外国救援人员直言:“现在金钱就如粪土,水才是货币”.下列是关于水的研究,请回答有关问题: A一G是初中常见的7种物质.它们有如下图所示的转化关系.其中:“一”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质(反应条件和部分反应物已经略去).已知A和C是由两种组成元素相同的无色液体,B、G是无色气体,绿色植物可将气体G通过光合作用吸收,并转化为无色气体B,E、F是黑色固体.D在纯B中剧烈燃烧,火星四射.请回答下列问题:
A一G是初中常见的7种物质.它们有如下图所示的转化关系.其中:“一”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质(反应条件和部分反应物已经略去).已知A和C是由两种组成元素相同的无色液体,B、G是无色气体,绿色植物可将气体G通过光合作用吸收,并转化为无色气体B,E、F是黑色固体.D在纯B中剧烈燃烧,火星四射.请回答下列问题: