题目内容
15. 如图所示,一物体悬挂在饱和氯化钠溶液中,要使弹簧秤读数保持不变,在恒温条件下,可向烧杯内的溶液中加入(悬挂物不参与反应)( )
如图所示,一物体悬挂在饱和氯化钠溶液中,要使弹簧秤读数保持不变,在恒温条件下,可向烧杯内的溶液中加入(悬挂物不参与反应)( )| A. | 同温度下的饱和氯化钠溶液 | B. | 水 | ||
| C. | 硝酸钾晶体 | D. | 氯化钠晶体 |
分析 根据在恒温条件下向烧杯内饱和的氯化钠溶液中加入物质,对溶液中溶质质量变化情况,推断对溶液密度的影响,运用粗浮力公式,分析浸没物质所受浮力的变化,判断弹簧秤示数的变化.
解答 解:A、向烧杯内的溶液中加入同温度下的饱和氯化钠溶液,溶液的密度不变,浮力不变,弹簧秤读数保持不变,故A正确;
B、向烧杯内的溶液中加入水,溶液的密度变小,浮力变小,弹簧秤读数大,故B错误;
C、向烧杯内的溶液中加入硝酸钾晶体,溶液的密度变大,浮力变大,弹簧秤读数变小,故C错误;
D、向烧杯内的溶液中加入氯化钠晶体,不再溶解,溶液的密度不变,浮力不变,弹簧秤读数不变,故D正确.
故选AD.
点评 本题为跨学科型简答,溶液的密度是把两个学科联系起来的纽带,通过化学变化而改变溶液的组成从而引起溶液密度的变化.

练习册系列答案
相关题目
5. 已知M、N分别是稀硫酸、氢氧化钠溶液中的一种.
已知M、N分别是稀硫酸、氢氧化钠溶液中的一种.
某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH,如图所示.
(1)M是氢氧化钠溶液,该反应的化学方程式是2NaOH+H2SO4═Na2SO4+2H2O.
(2)反应过程中,老师取a、b、c三处反应后的溶液,打乱顺序后,请同学们不测定溶液pH,用其他实验方法对三种溶液进行探究.小明和小红分别取其中一种溶液进行实验:小明向所取溶液中加入CuSO4溶液,观察到有蓝色沉淀生成.
结论:是a处溶液.
小红向少量另一种溶液中滴加酚酞溶液,观察到溶液呈无色.
结论:是b处或c处溶液.
为进一步确定该处溶液成分,小红又设计并完成如下实验:
剩余一种为b处溶液.
 已知M、N分别是稀硫酸、氢氧化钠溶液中的一种.
已知M、N分别是稀硫酸、氢氧化钠溶液中的一种.某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH,如图所示.
(1)M是氢氧化钠溶液,该反应的化学方程式是2NaOH+H2SO4═Na2SO4+2H2O.
(2)反应过程中,老师取a、b、c三处反应后的溶液,打乱顺序后,请同学们不测定溶液pH,用其他实验方法对三种溶液进行探究.小明和小红分别取其中一种溶液进行实验:小明向所取溶液中加入CuSO4溶液,观察到有蓝色沉淀生成.
结论:是a处溶液.
小红向少量另一种溶液中滴加酚酞溶液,观察到溶液呈无色.
结论:是b处或c处溶液.
为进一步确定该处溶液成分,小红又设计并完成如下实验:
| 实验步骤 | 实验现象 | 结论 |
| 为c处溶液,并推知溶液中的离子有Na+、H+、Cl-(填离子符号) |
6.下列物质中含有氧分子的是( )
| A. | 二氧化锰 | B. | 高锰酸钾 | C. | 氧化铜 | D. | 液氧 |
10.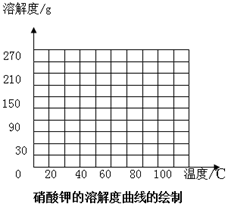 硝酸钾在不同温度时的溶解度如下:
硝酸钾在不同温度时的溶解度如下:
你能将硝酸钾的溶解度随温度变化的关系在图上表示出来吗?
 硝酸钾在不同温度时的溶解度如下:
硝酸钾在不同温度时的溶解度如下:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
20.在西部大开发中,投入了巨资兴建西气东输工程,将西部蕴藏的丰富资源,通过管道输送到东部地区,这里所指的西气主要成分是( )
| A. | CH4 | B. | CO | C. | H2 | D. | H2S |
5. “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图14所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,展开了实验探究.请你一起参与探究活动,并填写题中空白.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图14所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,展开了实验探究.请你一起参与探究活动,并填写题中空白.
【提出问题】久置“双吸剂”的成分是什么?
【做出猜想】久置“双吸剂”中可能有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究1】取固体样品研磨,用磁铁吸引,磁铁上沾有黑色粉末,说明“双吸剂”中一定有Fe.再用磁铁反复吸引后,残留固体用于后续探究活动.
【实验探究2】
【反思提高】
(1)请写出【探究2】操作3中所涉及的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)有同学提出【探究2】操作2中得出的结论不合理,理由是CaO+H2O=Ca(OH)2.(用方程式表示)
 “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图14所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,展开了实验探究.请你一起参与探究活动,并填写题中空白.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图14所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,展开了实验探究.请你一起参与探究活动,并填写题中空白.【提出问题】久置“双吸剂”的成分是什么?
【做出猜想】久置“双吸剂”中可能有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究1】取固体样品研磨,用磁铁吸引,磁铁上沾有黑色粉末,说明“双吸剂”中一定有Fe.再用磁铁反复吸引后,残留固体用于后续探究活动.
【实验探究2】
| 实验操作 | 实验现象 | 实验结论 |
| 1.将实验探究1中残留固体中加入足量水充分溶解 | 固体部分溶解,并放出热量 | 固体中一定含有CaO; |
| 2.过滤,向滤液中滴加几滴无色酚酞试液 | 无色变红色 | 固体中一定含有Ca(OH)2 |
| 3.取过滤后滤渣,加入足量稀盐酸 | 1.产生大量气泡 2.溶液由无色变为黄色 | 固体中一定有CaCO3和 Fe2O3. |
(1)请写出【探究2】操作3中所涉及的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)有同学提出【探究2】操作2中得出的结论不合理,理由是CaO+H2O=Ca(OH)2.(用方程式表示)
 如图是一瓶刚开启的“XX牌”碳酸饮料的示意图.请回答:
如图是一瓶刚开启的“XX牌”碳酸饮料的示意图.请回答: