题目内容
13.8.8克二氧化碳通入200克8%的氢氧化钠溶液中恰好完全反应.请回答下列问题:(1)反应后所得的溶液质量为208.8克.
(2)反应后所得的溶液的pH值>7.
(3)所得溶液的溶质质量分数是多少?
分析 二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠溶液和氢氧化钠溶液都是显碱性溶液,pH都大于7,根据反应的化学方程式及其提供的数据可以计算所得溶液的溶质质量分数.
解答 解:(1)反应后所得的溶液质量为:200g+8.8g=208.8g,
故填:208.8.
(2)反应后所得的溶液是碳酸钠溶液,碳酸钠溶液的pH>7.
故填:>.
(3)设生成碳酸钠质量为x,
2NaOH+CO2═Na2CO3+H2O,
44 106
8.8g x
$\frac{44}{8.8g}$=$\frac{106}{x}$,
x=21.2g,
所得溶液的溶质质量分数是:$\frac{21.2g}{208.8g}$×100%=10.2%,
答:所得溶液的溶质质量分数是10.2%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
4.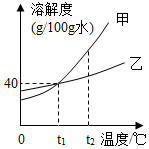 甲、乙两种固体均不含结晶水,在水中不发生反应且溶解性互不影响,它们的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种固体均不含结晶水,在水中不发生反应且溶解性互不影响,它们的溶解度曲线如图所示.下列说法正确的是( )
 甲、乙两种固体均不含结晶水,在水中不发生反应且溶解性互不影响,它们的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种固体均不含结晶水,在水中不发生反应且溶解性互不影响,它们的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃甲、乙的饱和溶液,降低温度,甲先析出晶体 | |
| B. | t1℃时,70g甲的饱和溶液加入40g乙物质,溶液质量仍为70g | |
| C. | 将t2℃甲、乙的饱和溶液分别降温至t1℃,析出晶体的质量:甲>乙 | |
| D. | 将t2℃等质量的甲、乙饱和溶液分别降温至t1℃,析出晶体的质量:甲>乙 |
18.关于离子和原子的关系说法错误的是( )
| A. | 离子是带电的原子或原子团,故从电性上看,原子不显电性,而离子显电性 | |
| B. | 离子是由原子得到或失去电子形成的 | |
| C. | 从结构上看,原子中核内质子数等于核外电子数,而在离子中两个数不相等 | |
| D. | 钠离子和钠原子的质子数相同,但它们不属于同种元素 |
3.下列选项的操作或反应所对应的曲线图正确的是( )
| A. | 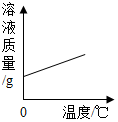 将饱和食盐水升温 | |
| B. | 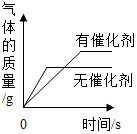 相同的两份H2O2溶液分解 | |
| C. |  一定量的锌粉与足量稀盐酸反应 | |
| D. | 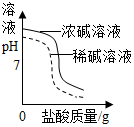 将同浓度的稀盐酸滴入等体积不同浓度的KOH溶液中 |