题目内容
14.现要制取一些二氧化氮气体来做演示分子运动的实验.已知二氧化氮气体可以通过铜和浓硝酸反应:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O得到.二氧化氮是一种红棕色的气体,密度比空气大,能和水反应生成HNO3和NO气体,NO和NO2都是大气污染物.现给出下列装置(A~F):
(1)制二氧化氮的发生装置可以选B,收集二氧化氮的装置可以选E;
(2)写出二氧化氮和水反应的化学方程式3NO2+H2O═2HNO3+NO;
(3)要得到干燥的二氧化氮可将其通过浓硫酸;
(4)NO一遇到O2就会变成NO2,收集NO应用排水法;
(5)用如上图F装置演示分子运动时,为了缩短演示的时间,NO2最好放在上(选填“上”或“下”)面的集气瓶中,另一瓶是空气,抽去两瓶之间的玻璃片,可以看到红棕色气体飘下,两个瓶子中都充满了红棕色气体,最后两瓶中气体颜色相同.
(6)小林同学用装置BC组合制取了一瓶无色无味纯净的气体,他制取的气体可能是CO2.
分析 (1)发生装置主要由反应物的状态和反应条件决定;收集装置主要由气体的密度和溶水性决定.
(2)根据题目中告诉的反应物、生成物、反应条件写出反应的化学方程式.
(3)常用的干燥剂一般有浓硫酸、固体氢氧化钠、氧化钙等.
(4)气体的收集装置主要由气体的密度和溶水性决定,另外还要考虑气体是否有毒、是否与空气反应、是否与水反应等等.
(5)从分子的性质进行分析;
(6)根据BC装置的特点解实验室中制取气体的反应原理进行解答.
解答 解:(1)反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置即选择B装置;二氧化氮是空气污染物,不能用排空气法收集,二氧化氮和水反应,不能用排水法收集,可用E装置收集,氢氧化钠溶液可以吸收多余的二氧化氮,防止污染空气.
(2)二氧化氮和水反应生成硝酸和一氧化氮,该反应的化学方程式为:3NO2+H2O═2HNO3+NO.
(3)浓硫酸具有吸水性,可用来干燥二氧化氮;
(4)一氧化氮会与空气中的氧气发生反应,还会污染空气,不能用排空气法收集,一氧化氮难溶于水,可用排水法收集;
(5)一切物质的分子都在不停的运动,将密度大的气体放在上面,密度小的气体放在下面会加快分子运动的速度,所以抽开纸片后能够发现红棕色气体飘下,两个瓶子中都充满了红棕色气体,最后两瓶中气体颜色相同;
(6)B装置为固液常温型的反应装置,而C为向上排气法收集气体的装置,在实验室中可以用该装置来制取二氧化碳.
故答案为:
(1)B;E;
(2)3NO2+H2O═2HNO3+NO;
(3)浓硫酸;
(4)排水;
(5)上;红棕色气体飘下,两个瓶子中都充满了红棕色气体,最后两瓶中气体颜色相同.
(6)CO2.
点评 在选择一种气体的收集方法时一定要考虑全面,这种气体的溶水性、是否与水反应、是否与空气中的某物质反应、密度、是否会污染空气等.要收集一瓶干燥的气体时一定要先干燥再收集.

 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案| A. | 泡菜 | B. | 苹果汁 | C. | 鸡蛋清 | D. | 西瓜汁 |
| A. |  鼻子闻 | B. |  嘴巴吹 | C. |  耳朵听 | D. |  眼睛看 |
| A. | 铝 | B. | 金刚石 | C. | NaCl | D. | NH3 |
| A. | 洗衣粉乳化油污 | B. | 厨房中煮饭菜用燃烧液化气 | ||
| C. | 风力发电 | D. | 海水晒盐 |

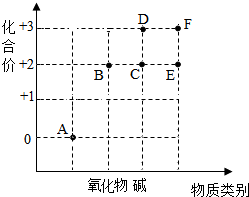 以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为铁 的价类图,则 E 点可表示+2价的亚铁盐.请回答:
以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为铁 的价类图,则 E 点可表示+2价的亚铁盐.请回答: