题目内容
水垢的主要成分为CaCO3,常加食醋进行除锈,其反应为2CH3COOH+CaCO3=(CH3COO)2Ca+H2O+CO2↑.如果加入10g食醋,恰好完全反应,物质的总质量减少2.2g,求所用食醋中醋酸的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:根据质量守恒定律可以知道,物质总质量减少的质量为二氧化碳的质量,结合醋酸和碳酸钙反应的化学方程式可以求算出醋酸的质量,进而求算出食醋中醋酸的质量分数.
解答:解:设所用的醋酸质量为X.
2CH3COOH+CaCO3═(CH3COO)2Ca+H2O+CO2↑
120 44
X 2.2g
=
X=6g
所用食醋中醋酸的质量分数是:
×100%=60%
答:所用食醋中醋酸的质量分数是60%.
2CH3COOH+CaCO3═(CH3COO)2Ca+H2O+CO2↑
120 44
X 2.2g
| 120 |
| X |
| 44 |
| 2.2g |
X=6g
所用食醋中醋酸的质量分数是:
| 6g |
| 10g |
答:所用食醋中醋酸的质量分数是60%.
点评:本题难度不是很大,主要考查了根据化学方程式进行相关的计算,从而培养学生的分析能力和计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某化学反应的微粒变化如图所示,下列有关判断正确的是( )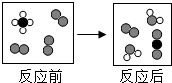

| A、反应物的化学计量数之比为1:1 |
| B、生成物中一定不含氧化物 |
| C、反应前后原子、分子数目没有变化 |
| D、反应类型为复分解反应 |
 A~D都是初中化学中的常见物质,C常温下是气态,且如图所示转化关系(反应条件、其他反应物及其他生成物均已略去):写出下列物质的化学式:
A~D都是初中化学中的常见物质,C常温下是气态,且如图所示转化关系(反应条件、其他反应物及其他生成物均已略去):写出下列物质的化学式: