题目内容
化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
【提出问题2】该氢氧化钠溶液是全部变质还是部分变质呢?
【猜想与假设】猜想1:氢氧化钠溶液部分变质. 猜想2:氢氧化钠溶液全部变质.
【查阅资料】(1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3═CaCO3↓+2NaCl
【实验探究2】
【实验结论】该氢氧化钠溶液 (填“部分”或“全部”)变质.
【反思与评价】(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案 (填“可行”或“不可行”).
【理解与应用】氢氧化钠溶液容易变质为 ,必须密封保存.实验室必须密封保存的药品还有很多,试另举一例: .
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡. | 有气泡冒出. | 氢氧化钠溶液一定变质了. |
【猜想与假设】猜想1:氢氧化钠溶液部分变质. 猜想2:氢氧化钠溶液全部变质.
【查阅资料】(1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3═CaCO3↓+2NaCl
【实验探究2】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡. | 说明原溶液中一定有碳酸钠. | |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. | 溶液变红色. | 说明原溶液中一定有 |
【反思与评价】(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案
【理解与应用】氢氧化钠溶液容易变质为
考点:药品是否变质的探究,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:由[实验探究2]知,(1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,溶液中的碳酸钠会与之反应生成碳酸钙白色沉淀.
(2)从(1)的结论可知原溶液中含有碳酸钠时,滴加氯化钙时一定会生成碳酸钙的白色沉淀,取步骤(1)试管中的少量上层清液,滴加酚酞溶液,溶液变红色.因碳酸钠已完全被氯化钙反应,所以说明原溶液中一定有氢氧化钠.
[实验结论]该氢氧化钠溶液部分变质.
[反思与评价]:(1)氢氧化钠溶液露置于空气中容易变质,主要是氢氧化钠与二氧化碳反应生成碳酸钠和水导致的,写出反应的方程式;
(2)根据氢氧化钙和碳酸钠反应产生沉淀的同时还产生氢氧化钠对氢氧化钠的检验产生干扰进行分析;
【理解与应用】】根据常见需要密封保存的物质回答;
(2)从(1)的结论可知原溶液中含有碳酸钠时,滴加氯化钙时一定会生成碳酸钙的白色沉淀,取步骤(1)试管中的少量上层清液,滴加酚酞溶液,溶液变红色.因碳酸钠已完全被氯化钙反应,所以说明原溶液中一定有氢氧化钠.
[实验结论]该氢氧化钠溶液部分变质.
[反思与评价]:(1)氢氧化钠溶液露置于空气中容易变质,主要是氢氧化钠与二氧化碳反应生成碳酸钠和水导致的,写出反应的方程式;
(2)根据氢氧化钙和碳酸钠反应产生沉淀的同时还产生氢氧化钠对氢氧化钠的检验产生干扰进行分析;
【理解与应用】】根据常见需要密封保存的物质回答;
解答:解:[实验探究1]知氢氧化钠溶液已变质,所以氢氧化钠溶液中含有碳酸根离子,因此加入盐酸必产生二氧化碳气体,反应的方程式为:2HCl+Na2CO3═2NaCl+H2O+CO2↑;
[实验探究2](1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,因碳酸钠与氯化钙能生成碳酸钙沉淀,所以有白色沉淀生成,说明原溶液中一定有碳酸钠;
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液,溶液变红色.溶液显碱性,因溶液中碳酸钠已被氯化钙完全消耗,所以说明原溶液中一定有氢氧化钠;
[实验结论]由以上的分析可知氢氧化钠溶液中既含氢氧化钠又含碳酸钠,因此是部分变质;
[反思与评价](1)氢氧化钠溶液露置于空气中容易与二氧化碳反应生成碳酸钠和水,相关反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;
(2)因为氢氧化钙和碳酸钠反应产生沉淀的同时还产生氢氧化钠对氢氧化钠的检验产生干扰,因此该方案不可行;
【理解与应用】氢氧化钠溶液容易与空气中的二氧化碳反应变质为碳酸钠,必须密封保存,因为浓盐酸具有挥发性,浓硫酸具有吸水性,因此都需要密封保存.
故答案为:[实验探究1]稀盐酸;产生气泡;2HCl+Na2CO3═2NaCl+H2O+CO2↑;
[实验探究2](1)白色沉淀;有氢氧化钠;
[实验结论]部分;
[反思与评价]:(1)CO2+2NaOH=Na2CO3+H2O;(2)不可行;
【理解与应用】碳酸钠、浓盐酸(或浓硫酸等).
[实验探究2](1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,因碳酸钠与氯化钙能生成碳酸钙沉淀,所以有白色沉淀生成,说明原溶液中一定有碳酸钠;
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液,溶液变红色.溶液显碱性,因溶液中碳酸钠已被氯化钙完全消耗,所以说明原溶液中一定有氢氧化钠;
[实验结论]由以上的分析可知氢氧化钠溶液中既含氢氧化钠又含碳酸钠,因此是部分变质;
[反思与评价](1)氢氧化钠溶液露置于空气中容易与二氧化碳反应生成碳酸钠和水,相关反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;
(2)因为氢氧化钙和碳酸钠反应产生沉淀的同时还产生氢氧化钠对氢氧化钠的检验产生干扰,因此该方案不可行;
【理解与应用】氢氧化钠溶液容易与空气中的二氧化碳反应变质为碳酸钠,必须密封保存,因为浓盐酸具有挥发性,浓硫酸具有吸水性,因此都需要密封保存.
故答案为:[实验探究1]稀盐酸;产生气泡;2HCl+Na2CO3═2NaCl+H2O+CO2↑;
[实验探究2](1)白色沉淀;有氢氧化钠;
[实验结论]部分;
[反思与评价]:(1)CO2+2NaOH=Na2CO3+H2O;(2)不可行;
【理解与应用】碳酸钠、浓盐酸(或浓硫酸等).
点评:此题是一道实验探究题,解题的关键是把握在证明氢氧化钠部分变质时,先除去氢氧化钠中的碳酸钠,然后再证明剩余溶液显碱性,才能说明氢氧化钠部分变质.

练习册系列答案
相关题目
当打开一个装有液态空气的容器盖,并将一根燃烧着的木条置于容器口上方时,观察到的现象是( )
| A、燃着的木条火焰熄灭 |
| B、燃烧得更旺 |
| C、先燃烧得更旺,后熄灭 |
| D、无明显变化 |
下列有关实验现象的描述,正确的是( )
| A、铁丝在氧气中剧烈燃烧、火星四射、生成白色固体 |
| B、磷在空气中燃烧,产生大量白烟 |
| C、硫在氧气中燃烧生成二氧化硫 |
| D、木炭在氧气中燃烧时,发出黄色火焰,生成黑色固体 |
人类生活需要的能量大部分来自于化学反应.下列能量的转化不是由化学变化产生的是( )
| A、脂肪在人体内氧化释放能量维持生命活动 |
| B、用锂电池给数码相机供电 |
| C、利用太阳能加热水 |
| D、使用液化石油气做饭 |
下列实验操作正确的是( )
A、 |
B、 |
C、 |
D、 |
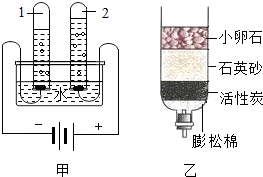 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.