题目内容
20.根据如图所示实验装置图回答问题:
(1)请填写标号仪器的名称:b锥形瓶.
(2)实验室用氯酸钾制备氧气的原理是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.如用F装置收集O2,气体应从②进入(填接口序号).
(3)实验室常用氯化铵固体与熟石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性.制取并收集NH3,应该从如图中选择的装置组合是A和D.
分析 (1)根据常见的化学仪器的名称,进行分析解答.
(2)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,结合氧气的密度比空气的大,进行分析解答.
(3)实验室常用氯化铵固体与熟石灰固体共热来制取氨气,氨气密度比空气小,极易溶于水,进行分析解答.
解答 解:(1)仪器b是锥形瓶.
(2)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
如用F装置收集O2,氧气的密度比空气的大,气体应从②进入,将空气从短导管排出.
(3)实验室常用氯化铵固体与熟石灰固体共热来制取氨气,属于固体加热型制取气体,应选用的制取装置是A;氨气密度比空气小,极易溶于水,应选用向下排空气法收集,应选用的收集装置是D.
故答案为:(1)锥形瓶;(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;②;(3)A和D.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取氧气的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.下列净化水的方法中,单一操作净化程度较高的是( )
| A. | 过滤 | B. | 沉淀 | C. | 吸附 | D. | 蒸馏 |
8.小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的.他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
【回答问题】(1)用砂纸打磨金属片的目的是除去金属片表面的氧化物或污物.
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是无法比较铬和铝的金属活动性强弱.
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是Al、CrSO4溶液、Cu等(合理即可).
【归纳】比较金属活动性强弱的方法有①利用金属和酸的反应判断金属活动性②利用金属和盐溶液的反应判断金属活动性.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验一 | 实验二 | 实验三 | |
| 实验 方案 |  |  | 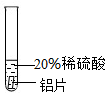 |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 无明显现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是Al>Cr>Cu | |||
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是无法比较铬和铝的金属活动性强弱.
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是Al、CrSO4溶液、Cu等(合理即可).
【归纳】比较金属活动性强弱的方法有①利用金属和酸的反应判断金属活动性②利用金属和盐溶液的反应判断金属活动性.
12.某校在春暖花开的四月组织了一次春游活动,下列为此次春游活动中的部分问题,请您帮助回答:
(1)有些同学带了如下的食品,其中主要为人体提供蛋白质的是A(填字母).
A.午餐肉 B.西红柿 C.面包 D.黄瓜
(2)还有同学料带来有如表标签的饮料.
该饮料中含有人体必须的微量元素是锌.
(3)野炊用水主要来自废黄河,你认为这样的水属于混合物(填“纯净物”或“混合物”).若要测定该水的酸碱度,可以选择C.
A.紫色石蕊试液 B.无色酚酞试液 C.pH试纸 D.蓝石蕊试纸
(4)在野炊活动过程中,小花不小心被蚂蚁(毒液蚁酸)咬了,下列物品可以用于涂抹以减轻疼痛的是C(选填下列字母).
A.氢氧化钠溶液 B.食盐水 C.肥皂水D.食醋
(5)在清理垃圾时发现一袋脱氧剂,拆开后看到是还原铁粉,但已部分生锈,该还原铁粉生锈的主要原理是Fe与潮湿的空气接触.
(1)有些同学带了如下的食品,其中主要为人体提供蛋白质的是A(填字母).
A.午餐肉 B.西红柿 C.面包 D.黄瓜
(2)还有同学料带来有如表标签的饮料.
| 营养成分 | 糖类 | 钠 | 钙 | 锌 | 维生素C | 维生素B6 |
| 含量/500mL | 22.5g | 16mg | 16mg | 3.0mg | 100mg | 0.56mg |
(3)野炊用水主要来自废黄河,你认为这样的水属于混合物(填“纯净物”或“混合物”).若要测定该水的酸碱度,可以选择C.
A.紫色石蕊试液 B.无色酚酞试液 C.pH试纸 D.蓝石蕊试纸
(4)在野炊活动过程中,小花不小心被蚂蚁(毒液蚁酸)咬了,下列物品可以用于涂抹以减轻疼痛的是C(选填下列字母).
A.氢氧化钠溶液 B.食盐水 C.肥皂水D.食醋
(5)在清理垃圾时发现一袋脱氧剂,拆开后看到是还原铁粉,但已部分生锈,该还原铁粉生锈的主要原理是Fe与潮湿的空气接触.
9.如图实验过程与图象描述不相符合的选项是( )
| A. |  向一定量的水中加入生石灰 | B. |  红磷在装有空气的密闭容器中燃烧 | ||
| C. |  向一定质量的烧碱溶液中滴入盐酸 | D. |  向饱和KNO3溶液中加入KMnO4固体 |
10.下列实验现象的描述,错误的是( )
| A. | 木炭在氧气中燃烧发出黄光 | |
| B. | 磷在氧气中燃烧生成白色固体 | |
| C. | 蜡烛在氧气中燃烧发出白光 | |
| D. | 硫在氧气中燃烧发出明亮的蓝紫色火焰 |
 如图1是A、B、C三种物质的溶解度曲线.请回答:
如图1是A、B、C三种物质的溶解度曲线.请回答: