题目内容
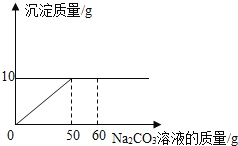
【题目】将14.4g含有NaCl和CaCl2的固体混合物,加入到45.6g的足量的水中,在所得溶液中逐滴加入一定溶质质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量与沉淀质量关系如图:(化学方程式 CaCl2+Na2CO3═CaCO3↓+2NaCl)
(1)求Na2CO3溶液的溶质质量分数_____;
(2)原混合溶液中CaCl2的质量_____;
(3)当CaCl2和Na2CO3恰好完全反应时,过滤,求所得溶液中溶质的质量分数_____。
【答案】21.2% 11.1g 15%
【解析】
由图像可知,恰好完全反应时,生成沉淀10g,消耗碳酸钠溶液50g;
设溶液中Na2CO3的质量为x,混合物中CaCl2的质量为y,生成NaCl的质量为z:
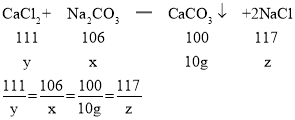
x=10.6g,y=11.1g,z=11.7g
(1)Na2CO3溶液的溶质质量分数:![]() ;
;
(2)CaCl2的质量为11.1g;
(3)所得溶液中溶质的质量分数为:![]()
答:(1)Na2CO3溶液的溶质质量分数为21.2%;
(2)CaCl2的质量为11.1g;
(3)所得溶液中溶质的质量分数为15%。

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目