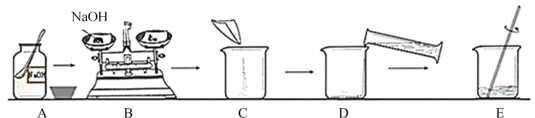
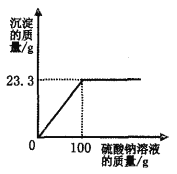
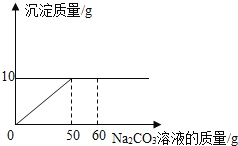
题目内容
【题目】下列各组离子能在碳酸钠溶液中大量共存的是( )
A. Na+,![]() ,OH﹣B. K+,Cu2+,OH﹣
,OH﹣B. K+,Cu2+,OH﹣
C. Zn2+,Na+,Cl﹣D. Ba2+,H+,![]()
【答案】A
【解析】
A、离子间若能互相结合生成沉淀、气体或水,则离子不能共存。 Na+,![]() ,OH﹣离子间不能结合成沉淀、气体或水,能大量共存,故选项正确;
,OH﹣离子间不能结合成沉淀、气体或水,能大量共存,故选项正确;
B、Cu2+、OH﹣两种离子能结合成氢氧化铜沉淀,不能大量共存,故选项错误;
C、碳酸钠溶液中有大量的CO32﹣,Zn2+与CO32﹣能结合生成碳酸锌沉淀,不能大量共存,故选项错误;
D、碳酸钠溶液中有大量的CO32﹣,Ba2+、H+与CO32﹣离子,分别能结合成碳酸钡沉淀、二氧化碳和水,不能大量共存,故选项错误。
故选:A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
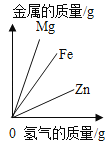
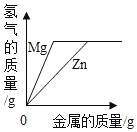
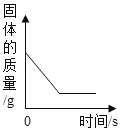
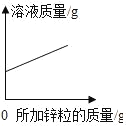
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
Mg、Zn、Fe与稀盐酸反应 | 等质量等质量分数的盐酸与足量的镁粉、锌粉 | 将铜片加入一定量的硝酸银溶液中 | 向一定质量的氯化锌和盐酸溶液中加入锌粒 |
A. A B. B C. C D. D