题目内容
16.浓硝酸和锌反应的化学方程式为Zn+4HNO3═Zn(NO3)2+2H2O+2X↑,则X为( )| A. | NH3 | B. | H2 | C. | NO | D. | NO2 |
分析 在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变.
解答 解:根据质量守恒定律和Zn+4HNO3=Zn(NO3)2+2H2O+2X↑可知,反应前锌原子是1个,反应后是1个;反应前氢原子是4个,反应后是4个;反应前氮原子是4个,反应后应该是4个,其中2个包含在2X中;反应前氧原子是12个,反应后应该是12个,其中4个包含在2X中;由分析可知,每个X中含有1个氮原子和2个氧原子,是二氧化氮,二氧化氮的化学式是NO2.
故选:D.
点评 判断X的化学式时,要注意X前面的化学计量数是2,2X中含有2个氮原子和4个氧原子,这样理解才不会出错.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目
6.下列实验操作正确的是( )
| A. | 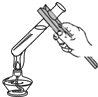 加热液体 | B. | 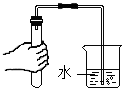 检查装置气密性 | C. | 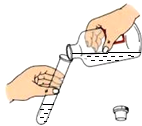 倾倒液体 | D. | 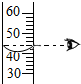 读取液体体积 |
7.某物质燃烧的反应方程式为X+302$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H20.由此判断X的化学式为( )
| A. | CH4 | B. | C2H6 | C. | C3H8 | D. | C2H5OH |
4.下列叙述错误的是( )
| A. | 绿色植物通过光合作用可以把太阳能转化为化学能 | |
| B. | 在化学反应X+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H20中X的化学式为C2H6 | |
| C. | 房屋失火用水扑灭是为了将燃烧物的温度降低到着火点以下 | |
| D. | 钢铁厂用赤铁矿炼铁的主要原理为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
1.为除去粗盐中的泥沙、CaCl2、MgCl2、Na2SO4杂质,得到NaCl,可先将粗盐溶于水,在进行以下操作:①过滤;②加过量的盐酸;③加过量的Na2CO3溶液;④加过量的NaOH溶液;⑤加过量的BaCl2溶液;⑥蒸发.正确的操作顺序是( )
| A. | ①④⑤③②⑥ | B. | ④⑤③①②⑥ | C. | ③④⑤①②⑥ | D. | ①⑤③④②⑥ |
5.下列各组物质的化学式、名称和分类三者不正确的是( )
| A. | CaO、生石灰、氧化物 | B. | CH4、沼气、有机物 | ||
| C. | Na2CO3、纯碱、碱 | D. | H3PO4、磷酸、酸 |
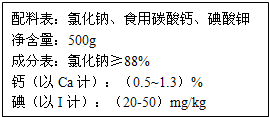 如图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算.
如图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算.