题目内容
15.某待测液中可能含有大量Mg2+、Cu2+、Fe3+、K+、H+、NO3-、SO42-、OH-离子中的一种或几种,现通过以下实验进行检验:(1)取少量待测液,仔细观察,呈无色;
(2)向上述待测液中逐渐滴加氢氧化钠溶液,先无明显现象,后有白色沉淀生成;
(3)向上述溶液中加入BaCl2溶液,无现象.
由上述实验得出的下列判断中,正确的是( )
| A. | 该待测液呈无色,Mg2+、Cu2+、Fe3+的溶液都有颜色,一定不能大量存在 | |
| B. | 该待测液中一定大量存在的离子是H+、Mg2+、NO3- | |
| C. | 该待测液中一定大量存在的离子是H+、Mg2+、NO3-、SO42- | |
| D. | 该待测液中不能确定存在的离子是K+、NO3- |
分析 (1)取少量待测液,仔细观察,呈无色,所以一定不含有Cu2+,Fe3+;
(2)向上述待测液中滴加NaOH溶液,先无明显现象,后有白色沉淀生成,则一定含有Mg2+,H+,一定不存在OH-;
(3)上述溶液中加入BaCl2溶液,无现象,一定不存在SO42-.
溶液显示中性,应该是阴阳离子均存在的,据此回答判断.
解答 解:A、Mg2+属于无色,Cu2+、Fe3+的溶液都有颜色,一定不能大量存在,故A错;
B、向上述待测液中滴加NaOH溶液,先无明显现象,后有白色沉淀生成,则一定含有Mg2+,H+,一定不存在OH-;上述溶液中加入BaCl2溶液,无现象,一定不存在SO42-.溶液显示中性,应该是阴阳离子均存在的,一定存在NO3-,故B正确;
C、上述溶液中加入BaCl2溶液,无现象,一定不存在SO42-.故C错;
D、取少量待测液,仔细观察,呈无色,所以一定不含有Cu2+,Fe3+;向上述待测液中滴加NaOH溶液,先无明显现象,后有白色沉淀生成,则一定含有Mg2+,H+,一定不存在OH-;上述溶液中加入BaCl2溶液,无现象,一定不存在SO42-.溶液显示中性,应该是阴阳离子均存在的,一定存在NO3-.综上:待测液中一定大量存在的离子是NO3-,Mg2+,H+,一定不能大量存在的离子是 Cu2+,Fe3+,SO42-,OH-,不能确定是否存在的离子是K+,故D错.
故选B.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水,难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
5.某化学兴趣小组的同学为测定某硫酸溶液的溶质质量分数,现称取100g该硫酸溶液放于烧杯中,然后向烧杯中逐滴滴加一定溶质质量分数的氯化钡溶液至恰好完全后过滤,记录实验数据如下表所示:
(1)反应后生成硫酸钡的质量是46.6克.
(2)请计算该硫酸溶液的溶质质量分数?
| 反应前 | 反应后 | ||
| 实验数据 | 硫酸溶液质量 | 氯化钡溶液质量 | 反应后溶液质量 |
| 100克 | 100克 | 153.4克 | |
(2)请计算该硫酸溶液的溶质质量分数?
6.生活中处处有化学,下列家庭小实验中不涉及化学变化的是( )
| A. |  柠檬酸、纯碱等制汽水 | B. |  木炭除去冰箱中异味 | ||
| C. |  食醋除去水垢 | D. |  探究铁生锈的条件 |
3.下列图示的实验操作中错误的是( )
| A. |  气密性的检查 气密性的检查 | B. | 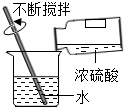 稀释浓硫酸 稀释浓硫酸 | ||
| C. |  铁丝在氧气中燃烧 铁丝在氧气中燃烧 | D. |  测定空气的组成 测定空气的组成 |
10.日常生活中的下列做法,利用了化学变化的是( )
| A. | 用洗衣粉洗去衣服上的油污 | |
| B. | 用酒精杀菌消毒 | |
| C. | 用硫酸钡做钡餐透视 | |
| D. | 用开水烫洗香椿芽去除其含有的亚硝酸盐 |
20.分类法是一种行之有效、简单易行的科学方法.某同学用如表所示形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系,下列各组中,有错误的组合是( )
| 选项 | 甲 | 乙 |
| A | 常见有机合成材料 | 塑料、合成橡胶、合成纤维 |
| B | 常见合金 | 不锈钢、焊锡、生铁 |
| C | 常见的化合物 | 干冰、蒸馏水、硫酸、胆矾 |
| D | 常见的碱 | 烧碱、生石灰、熟石灰 |
| A. | A | B. | B | C. | C | D. | D |
7.物质的下列用途主要利用其物理性质的是( )
| A. | 干冰用于人工降雨 | B. | 稀盐酸用于金属表面除锈 | ||
| C. | 白醋由于清除水壶中的水垢 | D. | 苏打水用于缓解胃酸过多 |
4.下列说法中,正确的是( )
| A. | 合金被广泛的使用,是因为合金比组成它们的纯金属具有更多优良性能 | |
| B. | 人体缺少必须微量元素会得病,因为应尽可能多吃含有这些元素的营养补剂 | |
| C. | 打开汽水瓶盖时,汽水会自动喷出来,说明此时气体在水中的溶解度变大了 | |
| D. | 一氧化碳有毒,燃着的煤炉会产生一氧化碳,在煤炉上放一壶水能防止人中毒 |
7.类推是化学学习中常用的思维方法.下列类推结果正确的是( )
| A. | 金刚石和石墨都是碳的单质,金刚石能作玻璃刀,所以石墨也能作玻璃刀 | |
| B. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| C. | SO2和CO2都能与水反应生成酸,所以SO2和CO2都能与NaOH溶液反应 | |
| D. | NaOH和Cu(OH)2都是碱,所以它们具有完全相同的性质 |