题目内容
实验室欲制取少量的FeCl3溶液.下列方案中你认为正确的是( )
| A、过量Fe和稀HCl反应后过滤 |
| B、过量Fe2O3和HCl反应后过滤 |
| C、过量HCl和Fe2O3反应后过滤 |
| D、过量Fe和CuCl2溶液反应后过滤 |
考点:酸的化学性质,金属的化学性质
专题:常见的酸 酸的通性
分析:根据金属活动性顺序和酸的性质进行分析.
解答:解:
A、Fe和稀HCl反应,生成氯化亚铁,而非氯化铁,故错误;
B、过量Fe2O3和HCl反应,生成氯化铁,过滤除掉氧化铁,故正确;
C、过量HCl和Fe2O3反应,生成氯化铁,也混有氯化氢,故错误;
D、过量Fe和CuCl2溶液反应,生成氯化亚铁,而非氯化铁,故错误.
故选:B.
A、Fe和稀HCl反应,生成氯化亚铁,而非氯化铁,故错误;
B、过量Fe2O3和HCl反应,生成氯化铁,过滤除掉氧化铁,故正确;
C、过量HCl和Fe2O3反应,生成氯化铁,也混有氯化氢,故错误;
D、过量Fe和CuCl2溶液反应,生成氯化亚铁,而非氯化铁,故错误.
故选:B.
点评:做题时一定要考虑铁在发生置换反应是只表现+2价,即生成亚铁离子.

练习册系列答案
相关题目
下列物质能由金属与酸直接反应生成的是( )
| A、CuCl2 |
| B、ZnCl2 |
| C、FeCl3 |
| D、AgCl |
下列选项中前者属于氧化物,后者属于混合物的是( )
| A、蒸馏水、洁净的海水 |
| B、镁条、石灰石 |
| C、稀硫酸、石灰水 |
| D、氧化钠、干冰 |
在天平的左右两个托盘上,各放一质量相等的烧杯,其中盛有等质量、等质量分数的稀硫酸,天平平衡,如果分别将下列四组中的两种物质放入左右两个烧杯内,充分反应后,天平仍保持平衡的是( )
| A、等质量的锌和铜 |
| B、等质量的锌和铁(反应后烧杯内酸都有剩余) |
| C、等质量的锌和铁(反应后烧杯中两种金属均有剩余) |
| D、等质量的氧化铜和铁 |
要配制质量分数为20%的硫酸溶液,需用质量分数分别为60%、10%的硫酸溶液的质量比为( )
| A、1:3 | B、1:5 |
| C、1:6 | D、1:4 |
我们肉眼年看得见的宏观变化,实际是因肉眼看不到的微观变化引起的.宏观与微观结合,有利于我们掌握化学知识.下列示意图表示某化学反应,其中相同的球代表同种原子.下列判断不正确的是( )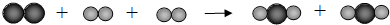
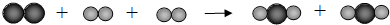
| A、化学反应前后原子种类、数目不变 |
| B、化学反应前后元素的种类、质量未发生变化 |
| C、该反应中,分子的个数比为1:2:2 |
| D、该反应不属于基本类型反应 |
 某同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图所示.经过一周观察:试管A和C当中的铁钉无明显变化,试管B中的铁钉明显锈蚀.
某同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图所示.经过一周观察:试管A和C当中的铁钉无明显变化,试管B中的铁钉明显锈蚀. 如图表示通电分解水的简易装置.试填写下列空白.
如图表示通电分解水的简易装置.试填写下列空白.