题目内容
9.在40℃时,取等质量的a、b、c三种物质的饱和溶液于三个烧杯中,再分别蒸发等质量的水,并将温度降到30℃,固体溶解情况如图1所示;图2为a、b、c三种物质的溶解度曲线,回答下列问题.(1)图2中P点的意义是在30℃时a和b的溶解度相等,三种物质溶解度关系为b>a>c时的温度为t,则t的取值范围是:20℃<t<30℃;
(2)40℃时,烧杯丙(填“甲”、“乙”或“丙”)里溶液中水量最少;根据图1析出固体质量的变化可推测烧杯甲里是b物质的溶液,烧杯乙里是c物质的溶液.
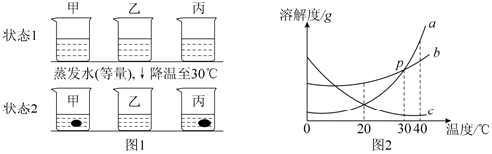
分析 由题意结合溶解度曲线可以确定可以确定三种物质的溶解度关系为b>a>c时的温度范围;根据降温后乙中没有剩余的固体,确定乙的溶解度随温度的降低而增大,故乙的曲线是c,丙析出的晶体多,故丙的溶解度受温度影响变化明显,故丙的曲线是a,据此解答.
解答 解:(1)由三物质的溶解度曲线不难看出,P点表示在30℃时a和b的溶解度相等;温度在20℃和30℃之间时,三物质的溶解度大小关系是b>a>c,故答案为:在30℃时a和b的溶解度相等;20℃<t<30℃.
(2)20℃时,b的溶解度最大,故等质量饱和溶液中含水最少的是b.
(3)在40℃时,取等质量的a、b、c三种物质的饱和溶液于三个烧杯中,再分别蒸发等质量的水,并将温度降到30℃,降温后乙中没有剩余的固体,确定乙的溶解度随温度的降低而增大,故乙的曲线是c,丙析出的晶体多,故丙的溶解度受温度影响变化明显,故丙的曲线是a,故甲的曲线是b,等质量的饱和溶液,溶解度越大,则需要的水的质量越少,故填:丙;b;c.
点评 本题难度不是很大,主要考查了固体溶解度曲线的作用,从而加深学生对固体溶解度的理解,培养学生分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列做法不正确的是( )
| A. | 购物时自带包装袋,减少塑料袋使用 | |
| B. | 可用氢氧化钠溶液区别浓硫酸和氯酸钾 | |
| C. | 饮食要少盐、控油 | |
| D. | 用pH试纸蘸取瓶内溶液测定溶液酸碱性 |
20.下列实验操作及现象合理的是( )
| A. | 用50mL量筒量取5.26mL水 | |
| B. | 硫粉在氧气中燃烧,产生淡蓝色火焰 | |
| C. | 镁与稀盐酸反应产生气体,放出热量 | |
| D. | 红磷在空气中燃烧,产生大量的白雾 |
17.在宏观和微观之间建立联系是化学学科特有的思维方式.下列宏观事实的微观解释错误的是( )
| A. | 10ml酒精和10ml水混合后体积小于20ml,混合后分子变小了 | |
| B. | 稀有气体可作保护气:原子核外电子达到相对稳定结构 | |
| C. | 水电解生成氢气和氧气:分子在化学变化中可以再分 | |
| D. | 氢氧化钠和氢氧化钙化学性质相似:溶液中都含有相同的阴离子氢氧根离子 |
14.某化合物R3.2g在空气中充分燃烧只生成8.8g二氧化碳和7.2g水,下列对化合物R的叙述中正确的是( )
| A. | R由碳、氢、氧三种元素组成 | B. | R中碳、氢、氧元素的质量比为2:6:1 | ||
| C. | R的化学式是CH4 | D. | R中碳、氢原子个数比为3:1 |
18.下列说法正确的是( )
| A. | 碳酸钠溶液是酸溶液 | |
| B. | 打开浓盐酸的试剂瓶,瓶口会产生白烟 | |
| C. | 用铁桶配制波尔多液 | |
| D. | 浓硫酸露置于空气中,溶质质量分数变小 |
 某同学将溶质质量分数为20%的氢氧化钠溶液逐滴滴入129.8g硫酸和硫酸铜的混合溶液中,直至过量.加人氢氧化钠溶液的质量(横轴)与混合溶液中溶质质量(纵轴)的关系如图所示.
某同学将溶质质量分数为20%的氢氧化钠溶液逐滴滴入129.8g硫酸和硫酸铜的混合溶液中,直至过量.加人氢氧化钠溶液的质量(横轴)与混合溶液中溶质质量(纵轴)的关系如图所示. 化学小组同学用下图所示装置(夹持仪器已略去)做了2个兴趣实验.每次实验时,打开止水夹,均可见C瓶内的水流入D中,B中有气泡逸出.
化学小组同学用下图所示装置(夹持仪器已略去)做了2个兴趣实验.每次实验时,打开止水夹,均可见C瓶内的水流入D中,B中有气泡逸出.