题目内容
12.某工厂欲从只含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图: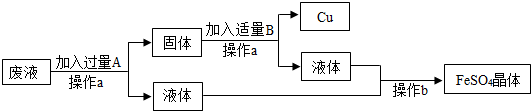
(1)操作a、b的名称分别是过滤、蒸发.
(2)写出流程中有关反应的化学方程式:Fe+CuSO4=FeSO4+Cu、Fe+H2SO4=FeSO4+H2↑.以上两个反应能够发生的原因是在金属活动性顺序中,铁位于铜、氢之前.
分析 在金属活动性顺序中,氢前的金属能与酸反应生成盐和氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,故要回收铜得到硫酸亚铁,可以加入铁.
解答 解:(1)经过操作a能得到固体和液体,所以a操作为过滤,从液体中得到晶体可以是蒸发操作;
(2)经过操作a得到的液体中能得到硫酸亚铁,说明回收铜时加入的是铁,多余的铁与硫酸反应生成硫酸亚铁,化学方程式为:Fe+CuSO4═FeSO4+Cu,Fe+H2SO4═FeSO4+H2↑.
故答案为:(1)过滤,蒸发;
(2)Fe+CuSO4═FeSO4+Cu,Fe+H2SO4═FeSO4+H2↑,在金属活动性顺序中,铁位于铜、氢之前.
点评 本题考查了铜的回收,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
2.通过实验可以获取证据,得出结论.下列做法中不能获得明显证据的是( )
| A. | 为了证明氢氧化钠溶液呈碱性,在其溶液中滴加稀盐酸 | |
| B. | 为了证明浓盐酸具有挥发性,打开盛浓盐酸的瓶盖,可以发现有“白雾” | |
| C. | 为了说明盐溶液不一定都呈中性,在碳酸钠溶液中滴加酚酞试液 | |
| D. | 为了证明汗水中含有Cl-,加入含稀硝酸的硝酸银溶液 |
3.下列关于氧气的叙述:①氧气能自燃;②氧气能支持燃烧;③氧气能与许多物质反应;④氧气能灭火;⑤有氧气参加的反应不一定是化合反应,其中正确的是( )
| A. | ①②⑤ | B. | ②③⑤ | C. | ①③⑤ | D. | ①③④ |
20.已知硝酸钾的溶解度随温度升高而增大,把一定量50℃的硝酸钾饱和溶液降温至30℃时,肯定不变的是( )
| A. | 溶质的质量 | B. | 溶液的质量 | ||
| C. | 溶液中溶质的质量分数 | D. | 溶剂的质量 |
7.今年入春至四月中旬,沈阳旱情严重,政府组织开展了较多的人工降雨活动.下列物质可用于人工降雨的是( )
| A. | 食盐 | B. | 干冰 | C. | 碳酸钠 | D. | 氯化钾 |
4.向含CaCl2、HCl二种溶质的溶液中加入10%的Na2CO3溶液实验过程中,加入Na2CO3溶液与产生沉淀或气体的关系如图1所示,加入Na2CO3溶液与溶液PH值变化如图2所示,则下列说法正确的是( )
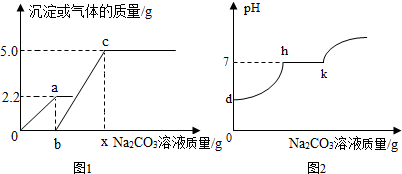

| A. | 图1中b→c段表示生成气体的过程 | |
| B. | 图1中b点的值为106 | |
| C. | 图1中c时溶液中有二种溶质 | |
| D. | 图1中0→a段反应过程中溶液PH值变化过程可用图2中d→h段表示 |
1.聚乳酸,一种可降解塑料,可用作包装材料、纤维和非织造物等.聚乳酸塑料属于( )
| A. | 无机非金属材料 | B. | 金属材料 | C. | 合成材料 | D. | 复合材料 |