题目内容
1.今年5月26日,广东省湛江市发生了2吨98%的浓硫酸意外泄露事件.当时恰逢阴雨天.因此产生了大量的酸雾,使九十多人中毒、灼伤.但是仍然有许多人利用身边的日常条件采取了防护措施,在很短的时间内从酸雾中逃生.请回答:(1)在阴雨天产生酸雾的原因是浓硫酸溶于水时产生大量的热,水受热蒸发.
(2)你认为逃生的人采取的防护措施是将碱面溶于水浇到自己身上,其中的道理是酸溶液可以和碱性溶液反应.
分析 (1)根据浓硫酸的性质进行分析;
(2)根据酸的性质进行分析解答即可.
解答 解:(1)2吨98%的浓硫酸泄露,当时恰逢阴雨天,浓硫酸溶于水时产生大量的热,水受热蒸发,因此产生了大量的酸雾,使九十多人中毒、灼伤,故填:浓硫酸溶于水时产生大量的热,水受热蒸发;
(2)根据酸溶液可以和碱性溶液反应的性质,可以将碱面溶于水浇到自己身上,从而减轻酸的伤害,故填:将碱面溶于水浇到自己身上;酸溶液可以和碱性溶液反应.
点评 此题难度不大,掌握浓硫酸的性质是解决此题的关键所在.

练习册系列答案
相关题目
9.下列关于固态物质的饱和溶液的说法中,正确的是( )
| A. | 饱和溶液就是不能继续溶解溶质的溶液 | |
| B. | 同一溶液的饱和溶液一定比其不饱和溶液浓 | |
| C. | 饱和溶液一定是浓溶液 | |
| D. | 饱和溶液在一定条件下可转化为不饱和溶液 |
16.已知在反应2A+B=2C中,参加反应的A、B的质量分别是10克和8克,生成的C的质量是( )
| A. | 2×10克+8克=28克 | B. | 10克+8克=18克 | ||
| C. | (2×10克+8克)÷2克=14克 | D. | (10克+8克)÷2=9克 |
6.化学研究的核心内容是( )
| A. | 物体的运动规律和光电现象 | B. | 生命有机体的形成及功能 | ||
| C. | 物质的组成、结构、性质和变化规律 | D. | 矿产资源、地域分布和自然环境 |
10.下列化学方程式符合题意且书写正确的是( )
| A. | 氢气作燃料无污染:2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| B. | 盐酸除铁锈:FeO+2HCl═FeCl2+H2O | |
| C. | 改良酸性土壤的原理:NaOH+HCl═NaCl+H2O | |
| D. | 用磷制作烟幕弹的原理:P+O2$\frac{\underline{\;点燃\;}}{\;}$ P2O5 |
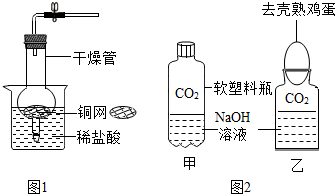 CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质: