题目内容
17.初三某化学小组的同学们学习“中和反应”后,在实验室里他们将一定量的氢氧化钠溶液与稀硫酸混合,如图1所示,其反应的化学方程式为2NaOH+H2SO4=Na2SO4+2H2O;同学们发现该反应没有明显的现象,进行了如下实验探究.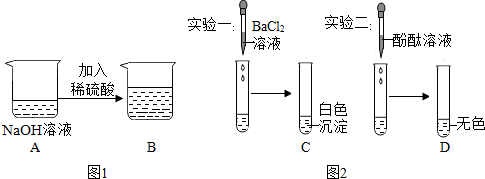
【提出问题1】如何验证该反应已经发生?
【进行实验】同学们分别取图1B图中溶液进行以下两个实验,结果如图所示:
【反应评价】你认为上述实验能验证反应已经发生的是实验二,请选择上述任一实验从微观角度分析其正确或错误的理由实验一中${SO}_{4}^{2-}$不参加反应(或实验二中可证明OH-全部反应).
【提出问题2】图1B图溶液中溶质的成分有哪些?
【进行实验】
| 实验操作 | 实验现象 | 结论 |
| 取B图中的少量溶液于试管中加入紫色石蕊溶液 | 观察到紫色石蕊变红 | B图中溶液的溶质是Na2SO4和H2SO4 |
【拓展延伸】将C图试管中的物质静置,上层清液中一定含有的溶质是NaCl、HCl.
分析 根据化学方程式的写法以及中和反应的过程来分析;
【反思评价】根据溶液酸碱性的变化以及微观反应的实质来分析;
【进行实验】根据酸的性质来分析;
【拓展延伸】根据C图的变化来分析.
解答 解:氢氧化钠与硫酸发生中和反应生成硫酸钠和水,故填:2NaOH+H2SO4=Na2SO4+2H2O;
【反思评价】氢氧化钠溶液显碱性,能使无色的酚酞试液变红色,但是加入稀硫酸后,不变色,说明其中的氢氧化钠参与了反应;实验一无法证明二者发生了反应,因为其中的硫酸根离子没有参与反应,滴加氯化钡溶液一定会产生白色沉淀或实验二可证明,因为酚酞试液变成了无色,说明氢氧根离子完全参与了反应;故填:二;实验一中${SO}_{4}^{2-}$不参加反应(或实验二中可证明OH- 全部反应);
【进行实验】要检验是否有硫酸的存在,可加入紫色的石蕊试液来检验,若溶液中滴加紫色的石蕊试液,变成了红色,则证明存在硫酸,也可加入铁粉或碳酸钠粉末,若有气泡产生,则证明有硫酸的存在;故填:紫色石蕊溶液;紫色石蕊变红;铁粉或Na2CO3(合理即可)
【拓展延伸】
硫酸与氢氧化钠反应生成了硫酸钠和水,向其中滴加氯化钡溶液,生成了硫酸钡白色沉淀和氯化钠;因为硫酸过量,所以硫酸与氯化钡溶液反应生成硫酸钡白色沉淀和盐酸;所以溶液中存在氯化钠和氯化氢两种溶质.故填:NaCl、HCl.
点评 本题为典型的实验探究中的实验分析题,只有熟练掌握所学知识才能明白实验的设计,才能顺利得出正确答案.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
5.下列实验方案,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别氧气、二氧化碳、氮气 | 燃着的木条分别伸入三种气体中 |
| B | 除去氯化钾溶液中的少量氯化铵 | 滴加适量氢氧化钠溶液 |
| C | 区别涤纶制品和纯棉制品 | 灼烧、观察是否能燃烧 |
| D | 验证盐酸中的H+能使紫色石蕊溶液变红 | 将紫色石蕊溶液分别滴入蒸馏水、 稀盐酸、氯化钠溶液中 |
| A. | A | B. | B | C. | C | D. | D |
8.实验设计时化学实验的重要环节,请根据下列实验要求回答相关问题:
【活动与探究一】用对比实验方法探究二氧化碳的性质.
(1)实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;对比A瓶与C(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
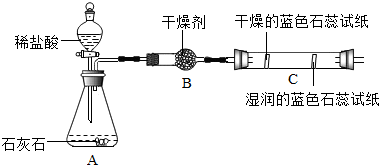
(2)实验二观察到C装置中发生的现象是干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色,结论是CO2+H2O=H2CO3(用化学方程式表示).
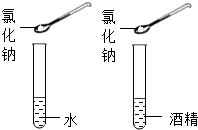
【活动与探究二】用变量控制方法探究影响物质溶解性的因素.
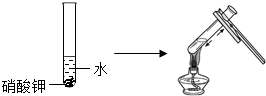
(3)实验三目的是探究温度对硝酸钾溶解性的影响;实验四是探究溶剂种类对物质溶解性的影响,该实验中需要控制的变量是温度和溶质、溶剂的质量相等.
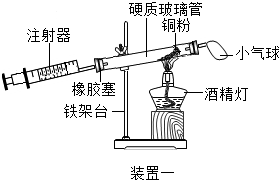
【活动与探究三】定量测定空气中氧气的含量.
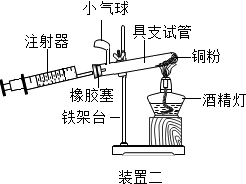
(4)实验五中,反应的原理为2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO(用化学方程式表示);装置一比装置二更合理,理由是装置一中氧气反应的更充分;
根据下表提供的实验数据,完成下表:
定量实验操作中易产生误差,如果反应前气球中存在气体(其量小于注射器内的空气),而实验后冷却至室温,将气球内的气体全部挤出读数,导致实验测得结果偏小(填“偏小”、“偏大”或“无影响”).
| 实验一 | 实验二 |
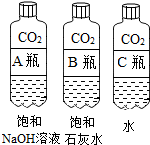 |  |
(1)实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;对比A瓶与C(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
(2)实验二观察到C装置中发生的现象是干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色,结论是CO2+H2O=H2CO3(用化学方程式表示).
【活动与探究二】用变量控制方法探究影响物质溶解性的因素.
| 实验三 | 实验四 |
 |  |
【活动与探究三】定量测定空气中氧气的含量.
| 实验五 | |
 |  |
根据下表提供的实验数据,完成下表:
| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 30mL | 20mL | 12mL | 16% |
5.进行化学实验操作考核时,下列四位同学的操作中正确的是( )
| A. |  检验溶液酸碱性 | B. |  溶解固体 | C. |  倾倒液体 | D. |  熄灭酒精灯 |
2.NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划分为一类物质,下列分类标准正确的是( )
| A. | 可与硝酸反应 | B. | 含钠的化合物 | C. | 溶于水的氧化物 | D. | 盐类物质 |
9.下列物质的利用对人体健康没有危害的是( )
| A. | 福尔马林浸泡海鲜 | B. | 用氮气给食品保鲜 | ||
| C. | 用工业酒精勾兑白酒 | D. | 大量使用亚硝酸钠腌制肉类 |
7.下列实验操作中,正确的是( )
| A. |  塞紧橡胶管 | B. |  倾倒液体 | C. |  加入固体 | D. |  加热 |
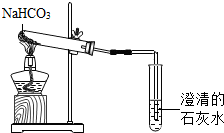 碳酸氢钠是一种重要的盐类物质,俗称小苏打,在生活中用途广泛,试举出碳酸氢钠在生活中的一种用途治疗胃酸的药物.
碳酸氢钠是一种重要的盐类物质,俗称小苏打,在生活中用途广泛,试举出碳酸氢钠在生活中的一种用途治疗胃酸的药物.