题目内容
14.闭容器中将20g氢气和氧气的混合气体点燃,发现剩余氢气2g,则原混合气体中氢气和氧气的质量比为( )| A. | 1:9 | B. | 1:8 | C. | 1:4 | D. | 1:2 |
分析 根据氢气在氧气中燃烧的化学方程式,由质量守恒定律,计算出生成水的质量,进而计算出参加反应的氢气和氧气的质量,进行分析解答即可.
解答 解:将20g氢气和氧气的混合气体点燃,发现剩余氢气2g,则生成水的质量为20g-2g=18g.
设参加反应的氢气和氧气的质量分别为x、y,
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O
4 32 36
x y 18g
$\frac{4}{36}=\frac{x}{18g}$ x=2g
$\frac{32}{36}=\frac{y}{18g}$ y=16g
由题意,剩余氢气2g,则反应前混合气体中含氢气2g+2g=4g,原混合气体中氢气和氧气的质量比为4g:16g=1:4.
故选:C.
点评 本题难度不是很大,考查学生利用化学反应方程式的计算来分析混合物的成分,利用化学反应判断恰好完全反应的量是正确解题的关键.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
4.下列有关催化剂的说法中正确的是( )
| A. | 加入二氧化锰可使过氧化氢溶液更快地产生氧气 | |
| B. | 二氧化锰是所有反应的催化剂 | |
| C. | 二氧化锰可使氯酸钾在常温下迅速产生氧气 | |
| D. | 催化剂一定能加快物质的反应速率 |
5.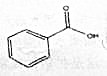 苯甲酸(化学式为C7H6O2)是重要的酸型食品防腐剂.在酸性条件下,对霉菌、酵母和细菌均有抑制作用.在食品工业用塑料桶装浓缩果汁、果酱(不包括罐头)、果汁(味)型饮料、酱油、食醋、软糖、果酒、酱菜、酱类、蜜饯、碳酸饮料中均有使用.下列关于苯甲酸的说法不正确的是( )
苯甲酸(化学式为C7H6O2)是重要的酸型食品防腐剂.在酸性条件下,对霉菌、酵母和细菌均有抑制作用.在食品工业用塑料桶装浓缩果汁、果酱(不包括罐头)、果汁(味)型饮料、酱油、食醋、软糖、果酒、酱菜、酱类、蜜饯、碳酸饮料中均有使用.下列关于苯甲酸的说法不正确的是( )
 苯甲酸(化学式为C7H6O2)是重要的酸型食品防腐剂.在酸性条件下,对霉菌、酵母和细菌均有抑制作用.在食品工业用塑料桶装浓缩果汁、果酱(不包括罐头)、果汁(味)型饮料、酱油、食醋、软糖、果酒、酱菜、酱类、蜜饯、碳酸饮料中均有使用.下列关于苯甲酸的说法不正确的是( )
苯甲酸(化学式为C7H6O2)是重要的酸型食品防腐剂.在酸性条件下,对霉菌、酵母和细菌均有抑制作用.在食品工业用塑料桶装浓缩果汁、果酱(不包括罐头)、果汁(味)型饮料、酱油、食醋、软糖、果酒、酱菜、酱类、蜜饯、碳酸饮料中均有使用.下列关于苯甲酸的说法不正确的是( )| A. | 苯甲酸分子中C、H、O三种元素的原子个数比为7:6:2 | |
| B. | 苯甲酸中氢元素的质量分数最小 | |
| C. | 一个苯甲酸中含有7个碳原子、6个氢原子和2个氧原子 | |
| D. | 苯甲酸是多原子分子构成的化合物 |
3.下列气体中,属于纯净物的是( )
| A. | 洁净的空气 | B. | 汽车的尾气 | C. | 二氧化碳 | D. | 香烟的烟气 |