题目内容
6.如图为工业上利用石灰石和食盐水制作漂白粉的流程图.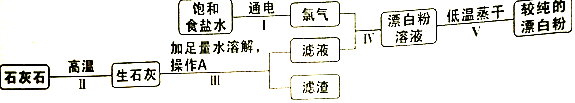
(1)石灰石高温煅烧得到两种氧化物,反应的化学方程式为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,步骤Ⅰ涉及到的能的转化是电能转化为化学能.
(2)请写出操作A用到的一种玻璃仪器的名称烧杯,步骤Ⅲ得到的滤液中的溶质是Ca(OH)2.
(3)漂白粉的主要成分是CaCl2和Ca(ClO)2,其中Ca(ClO)2中氯元素的化合价是+1.
(4)步骤Ⅴ采用低温蒸干,由此你推断处漂白粉的成分可能具有的一点性质是热不稳定性.
分析 (1)根据碳酸钙在高温的条件下生成氧化钙和二氧化碳,饱和氯化钠溶液通电生成氯气涉及到的能的转化是:电能转化为化学能进行分析;
(2)根据溶解过程中用到的玻璃仪器是烧杯、玻璃棒,水和氧化钙反应生成氢氧化钙进行分析;
(3)根据化合价代数和为零进行分析;
(4)根据步骤Ⅴ采用低温蒸干进行分析.
解答 解:(1)碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3 $\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑,饱和氯化钠溶液通电生成氯气涉及到的能的转化是:电能转化为化学能;
(2)溶解过程中用到的玻璃仪器是烧杯、玻璃棒,水和氧化钙反应生成氢氧化钙,所以步骤Ⅲ得到的滤液中的溶质是:Ca(OH)2;
(3)在次氯酸钙中,设氯元素的化合价为x,则+2+(x-2)×2=0,所以x=+1;
(4)步骤Ⅴ采用低温蒸干,所以漂白粉的成分可能具有的一点性质是热不稳定性.
故答案为:(1)CaCO3 $\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑,电能转化为化学能;
(2)烧杯,Ca(OH)2;
(3)+1;
(4)热不稳定性.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.韭菜是一种含铁量很高的蔬菜,每100克韭菜中含铁 8.9毫克.这里的“铁”指的是( )
| A. | 铁元素 | B. | 铁单质 | C. | 氧化铁 | D. | 铁的化合物 |
11.下列物质加入水中显著地放热的是( )
| A. | 固体氢氧化钠 | B. | 生石灰 | C. | 无水乙醇 | D. | 固体硝酸铵 |
18.下列实验操作能达到实验目的是A
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中少量的CO | 通过灼热的氧化铜粉末 |
| B | 除去CuSO4溶液中的少量FeSO4 | 加入足量的铜粉 |
| C | 鉴别澄清石灰水和NaOH溶液 | 加入稀盐酸 |
| D | 鉴别硬水和软水 | 加入肥皂水 |

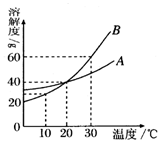 如图所示为 A、B两种固体物质的溶解度曲线.
如图所示为 A、B两种固体物质的溶解度曲线.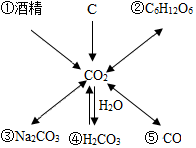 对物质进行归纳、分类、是学习化学的重要方法,如图是一位同学整理的有关CO2的知识网络图:
对物质进行归纳、分类、是学习化学的重要方法,如图是一位同学整理的有关CO2的知识网络图: