题目内容
20.现在下列实验装置,如图所示.回答问题
(1)仪器①的名称是试管.
(2)如果用氯酸钾和二氧化锰的混合物来制氧气,反应方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑可选用的发生装置是A.为了收集到不含空气的氧气,应选择的收集装置是F.
(3)质量分数为3%的医用双氧水在常温下难分解;但在双氧水溶液中加入铁锈,就会迅速分解,且反应结束后过滤出的铁锈可重复使用.试写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,反应类型为分解反应铁锈是该反应的催化剂;反应的发生装置为B.
(4)某学生利用烧杯、球形干燥管和单孔橡皮塞组成制取二氧化碳气体的装置(如图H所示).
①该装置A中应盛放的药品是稀盐酸,B处应放进石灰石或大理石.
②若使正在发生的反应停止,可以通过操作关闭止水夹C或将干燥管从烧杯中提出来实现.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气,该反应的反应物是固体,反应条件是加热,排水法收集的氧气纯净,排空气法收集的氧气干燥进行分析;
(3)根据过氧化氢在二氧化锰的催化作用下分解生成水和氧气,该反应是一种物质生成多种物质的反应,二氧化猛是该反应的催化剂,起催化作用,该反应的反应物是固体和液体,反应条件是常温进行分析;
(4)①根据实验室制取二氧化碳的反应物是稀盐酸和碳酸钙反应进行分析;
②根据固体忽然液体分离可以使反应停止进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是试管;
(2)氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,该反应的反应物是固体,反应条件是加热,所以选用的发生装置是:A,排水法收集的氧气纯净,排空气法收集的氧气干燥,所以应选择的收集装置是:F;
(3)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应是一种物质生成多种物质的反应,属于分解反应,二氧化猛是该反应的催化剂,起催化作用,所以反应的发生装置为:B;
(4)①通过分析可知,该装置A中应盛放的药品是稀盐酸,B处应放进石灰石和大理石;
②若使正在发生的反应停止,可以通过操作:关闭止水夹C或将干燥管从烧杯中提出来实现.
故答案为:(1)试管;
(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,A,F;
(3)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,分解反应,催化,B;
(4)①稀盐酸,大理石或石灰石;
②关闭止水夹C或将干燥管从烧杯中提出.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

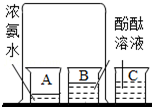 第二章课本中有一个“活动与探究”实验,其实验步骤是:将酚酞溶液分别倒入B、C两个小烧杯中,另取一个小烧杯A,加入约5mL浓氨水.用一个大烧杯罩住A、B两个小烧杯(如图所示)
第二章课本中有一个“活动与探究”实验,其实验步骤是:将酚酞溶液分别倒入B、C两个小烧杯中,另取一个小烧杯A,加入约5mL浓氨水.用一个大烧杯罩住A、B两个小烧杯(如图所示)(1)请你填写下表中的空白;
| 烧杯B | 烧杯C | |
| 现象 | ||
| 解释 | (此处不必填写) |
| 污染指数 | 50以下 | 51-100 | 101-150 | 151-200 | 201-250 | 251-300 | 300以上 |
| 质量级别 | Ⅰ | Ⅱ | Ⅲ(1) | Ⅲ(2) | Ⅳ(1) | Ⅳ(2) | Ⅴ |
| 质量状况 | 优 | 良 | 轻微污染 | 轻度污染 | 中度污染 | 中度重污染 | 重度污染 |
| A. | Ⅰ级 优 | B. | Ⅱ级 良 | C. | Ⅲ级 轻度污染 | D. | V级 重度污染 |
| A. | 溶质的质量分数都减小 | B. | 溶剂质量都增大 | ||
| C. | 溶液质量都增大 | D. | 溶质质量都减少 |
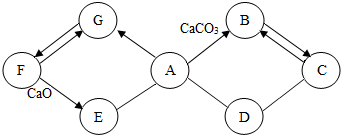
 钙元素对人类生命和生活具有重要意义:
钙元素对人类生命和生活具有重要意义:
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.