题目内容
往26g某合金中加入足量的稀盐酸,充分反应后得2g H2,则该合金可能的组成是( )
| A、Fe、Al | B、Fe、C |
| C、Cu、Fe | D、Mg、Al |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:解答此题首先根据极值法,将合金的质量认为是纯物质的质量,看能产生多少氢气,然后利用近似平均值法,合金产生的氢气的质量介于纯物质产生的氢气质量之间即可.
解答:解:设26g纯铁生成氢气的质量为x
Fe+H2SO4═FeSO4+H2↑
56 2
26g x
=
x≈0.9g
设26g纯铝生成的氢气质量为y
2Al+3H2SO4═Al2(SO4)3+3H2↑
54 6
26g y
=
y≈2.9g
设26g纯镁生成氢气的质量为a
Mg+H2SO4═MgSO4+H2↑
24 2
26g a
=
a≈2.2g
A、合金产生氢气的质量为2g,铁产生氢气的质量为0.9g,铝产生的氢气的质量为2.9g,介于混合金属之间,故A合理;
B、合金产生氢气的质量为2g,铁产生氢气的质量为0.9g,碳不产生氢气,故B不合理;
C、合金产生氢气的质量为2g,铁产生氢气的质量为0.9g,铜不产生氢气,故C不合理;
D、合金产生氢气的质量为2g,镁产生氢气的质量为2.2g,铝产生的氢气质量为2.9g,均大于合金产生的氢气的质量,故D不合理;
故选A.
Fe+H2SO4═FeSO4+H2↑
56 2
26g x
| 56 |
| 26g |
| 2 |
| x |
设26g纯铝生成的氢气质量为y
2Al+3H2SO4═Al2(SO4)3+3H2↑
54 6
26g y
| 54 |
| 26g |
| 6 |
| y |
设26g纯镁生成氢气的质量为a
Mg+H2SO4═MgSO4+H2↑
24 2
26g a
| 24 |
| 26g |
| 2 |
| a |
A、合金产生氢气的质量为2g,铁产生氢气的质量为0.9g,铝产生的氢气的质量为2.9g,介于混合金属之间,故A合理;
B、合金产生氢气的质量为2g,铁产生氢气的质量为0.9g,碳不产生氢气,故B不合理;
C、合金产生氢气的质量为2g,铁产生氢气的质量为0.9g,铜不产生氢气,故C不合理;
D、合金产生氢气的质量为2g,镁产生氢气的质量为2.2g,铝产生的氢气质量为2.9g,均大于合金产生的氢气的质量,故D不合理;
故选A.
点评:本题考查了混合金属产生氢气质量的有关判断,完成此题,可以依据极值法和近似平均值法进行.

练习册系列答案
相关题目
火箭所用的燃料是液态偏二甲肼(C2H8N2),氧化剂是N2O4.火箭工作中发生的反应为:
C2H8N2+2N2O4
2X↑+4H2O+3N2↑,则X的化学式是( )
C2H8N2+2N2O4
| ||
| A、CO |
| B、CO2 |
| C、C2O4 |
| D、C2O2 |
氯化钠和氯化镁混合溶于水后,加入适量的硝酸银溶液,加到不再有沉淀生成,滤去沉淀,再向滤液中加氢氧化钠溶液滤去沉淀,滤液用盐酸中和至中性,蒸发结晶后得到的物质是( )
| A、NaNO3 |
| B、Mg(NO3)2 |
| C、NaCl |
| D、MgCl2 |
下列做法可实现预期目标的是( )
| A、寻找新的催化剂使水变成汽油 |
| B、常用自来水冲洗自行车可防止生锈 |
| C、用氮气作焊接金属的保护气 |
| D、做测定空气中氧气含量的实验时,用蜡烛代替红磷 |
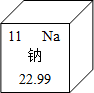 根据如图提供的信息判断,下列说法正确的是( )
根据如图提供的信息判断,下列说法正确的是( )| A、1个钠原子中有11个中子 |
| B、钠的原子序数为11 |
| C、钠属于非金属元素 |
| D、钠的相对原子质量是22.99g |
 炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可用图示进行实验:实验中玻璃管内的粉末由红色变为
炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可用图示进行实验:实验中玻璃管内的粉末由红色变为