题目内容
经初步测定知,某固体样品中可能含有FeO、Fe2O3、Fe3O4中的一种或几种成分,后又测知铁元素的质量分数为70%.则该固体样品可能有的组成为:
(有几种就填几种,可以不满)①只含有FeO;② ;③ .
(有几种就填几种,可以不满)①只含有FeO;②
考点:元素的质量分数计算
专题:化学式的计算
分析:根据题意铁元素的质量分数为70%,
根据FeO 中铁元素的质量分数,Fe2O3 中铁元素的质量分数,Fe3O4 中铁元素质量分数解答.
根据FeO 中铁元素的质量分数,Fe2O3 中铁元素的质量分数,Fe3O4 中铁元素质量分数解答.
解答:解:FeO 中铁元素的质量分数为
×100%=77.8%;Fe2O3 中铁元素的质量分数
×100%=70%;Fe3O4 中铁元素质量分数
×100%=72.4%;则该固体样品可能有的组成为:只有Fe2O3
答案:只有Fe2O3 不填
| 56 |
| 56+16 |
| 56×2 |
| 56×2+16×3 |
| 56×3 |
| 56×3+16×4 |
答案:只有Fe2O3 不填
点评:本题考查学生根据化合物中元素的质量比进行分析解题的能力;有两种或者是三种的话一定要一个比这个比例大,一个比这个比例小,混合物才能符合样品比例的条件.

练习册系列答案
相关题目
往26g某合金中加入足量的稀盐酸,充分反应后得2g H2,则该合金可能的组成是( )
| A、Fe、Al | B、Fe、C |
| C、Cu、Fe | D、Mg、Al |
下列是取出少量固体粉末并装入试管进行加热的过程,各步操作中正确的是( )
A、 取出固体粉末 |
B、 装入固体粉末 |
C、 点燃酒精灯 |
D、 加热固体粉末 |
如图是元素周期表中某元素的相关信息,从图中不能获得的信息是( )


| A、该元素是非金属元素 |
| B、该元素的原子序数为7 |
| C、该元素的相对原子质量是14.01 |
| D、氮气是无色无味的气体 |
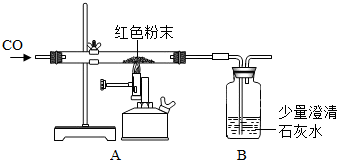 某化学兴趣小组同学在实验室找到一包“神秘的红色粉末”,老师提示说该红色粉末由Cu、Fe2O3二种固体中的一种或两种组成.该小组同学在教师指导下探究其组成.请你参与探究过程并回答有关问题.
某化学兴趣小组同学在实验室找到一包“神秘的红色粉末”,老师提示说该红色粉末由Cu、Fe2O3二种固体中的一种或两种组成.该小组同学在教师指导下探究其组成.请你参与探究过程并回答有关问题. 通常情况下,氨气(NH3)是一种无色.有刺激性气味的气体,密度比空气的小,极易溶于水,形成的溶液是氨水.实验室用加热氯化铵和消石灰的固体混合物制取氨气.如图是实验室常用的装置.请回答:
通常情况下,氨气(NH3)是一种无色.有刺激性气味的气体,密度比空气的小,极易溶于水,形成的溶液是氨水.实验室用加热氯化铵和消石灰的固体混合物制取氨气.如图是实验室常用的装置.请回答: