题目内容
12.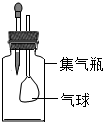 探究小组用如图装置进行实验.胶头滴管和集气瓶中分别盛装不同物质.挤压胶头滴管,向集气瓶中滴加适量液体后,能观察到气球变大的组合是( )
探究小组用如图装置进行实验.胶头滴管和集气瓶中分别盛装不同物质.挤压胶头滴管,向集气瓶中滴加适量液体后,能观察到气球变大的组合是( )| A. | 稀盐酸和石灰石 | B. | 水和氧化钙 | C. | 水和硝酸铵 | D. | 水和氢氧化钠 |
分析 观察到集气瓶中气球变大,说明集气瓶内压强减小,与大气相通的气球变大,根据每组物质的性质及变化规律,做出判断.
解答 解:A、向石灰石中滴加稀盐酸,盐酸与石灰石反应放出二氧化碳,放出气体使瓶内气体增多,气球变小;故A不正确;
B、向氧化钙中滴入水,氧化钙和水反应放出大量的热,放出的热使瓶内空气膨胀而使瓶内压强变大,气球变小;故B不正确;
C、硝酸铵溶于水会吸收热量,从而导致容器内的温度降低,所以能使瓶内气体压强减小,气球变大;故C正确;
D、向氢氧化钠中滴入水,氢氧化钠和水反应放出大量的热,放出的热使瓶内空气膨胀而使瓶内压强变大,气球变小;故D不正确;
故选C
点评 本题主要涉及盐酸和硝酸铵等物质的性质,正确掌握常见物质的性质,并熟练地运用性质解决问题是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.天津港爆炸救援时,防化团官兵深入爆炸核心区时应携带的物质是( )
| A. | 氧气 | B. | 臭氧 | C. | 二氧化碳 | D. | 氮气 |
20.某研究小组对“蜡烛在密闭装置中燃烧至熄灭,装置中是否有氧气剩余”进行了探究.
【提出问题】蜡烛在密闭装置中燃烧至熄灭,装置中是否有氧气剩余?
【猜想与假设】
猜想一:没有剩余;
猜想二:有剩余.
【设计并实验】
(1)气球的作用是缓冲集气瓶中的气压,防止瓶塞飞出.
(2)热水提供的热量就能引燃白磷,主要是利用白磷的着火点低的性质.
(3)白磷燃烧的现象是剧烈燃烧,产生大量白烟,放热,化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
【实验结论】
(4)根据①和②中的现象,得出的结论是蜡烛熄灭后,集气瓶中仍然含有氧气.
【拓展延伸】
(5)用氧气传感器定量测定密闭条件下足量白磷燃烧时氧气含量变化,如图3所示,在约90秒时氧气的含量有所上升,接着再慢慢下降,最终维持在8.0%左右,请你试着解释图象上氧气含量有所上升的主要原因是蜡烛燃烧产生的水蒸气液化.

【提出问题】蜡烛在密闭装置中燃烧至熄灭,装置中是否有氧气剩余?
【猜想与假设】
猜想一:没有剩余;
猜想二:有剩余.
【设计并实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 在底部铺有细沙的集气瓶中,放入一小块干燥的白磷,在集气瓶口的橡胶塞上安装一根玻璃管,在其上端系牢一个气球,点燃燃烧匙中蜡烛,迅速放入该集气瓶中 | 蜡烛逐渐熄灭 |
| ② | 蜡烛熄灭后,将集气瓶放入盛有热水的大烧杯中 | 白磷燃烧,产生大量白烟 |
(2)热水提供的热量就能引燃白磷,主要是利用白磷的着火点低的性质.
(3)白磷燃烧的现象是剧烈燃烧,产生大量白烟,放热,化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
【实验结论】
(4)根据①和②中的现象,得出的结论是蜡烛熄灭后,集气瓶中仍然含有氧气.
【拓展延伸】
(5)用氧气传感器定量测定密闭条件下足量白磷燃烧时氧气含量变化,如图3所示,在约90秒时氧气的含量有所上升,接着再慢慢下降,最终维持在8.0%左右,请你试着解释图象上氧气含量有所上升的主要原因是蜡烛燃烧产生的水蒸气液化.
7.下列关于溶液的说法正确的是( )
| A. | 无色透明的液体都是溶液 | |
| B. | 饱和溶液比不饱和溶液要浓 | |
| C. | 同一种溶质在不同溶剂中的溶解度相同 | |
| D. | 溶液析出晶体后,但溶液不一定变稀 |
1.以下关于燃烧与灭火的说法正确的是( )
| A. | 只有在点燃或加热时可燃物才能燃烧 | |
| B. | 只要温度达到可燃物着火点可燃物就能燃烧 | |
| C. | 只有含碳元素的物质才能燃烧 | |
| D. | 只要使可燃物的温度降到着火点以下就能灭火 |


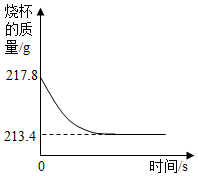 石家庄市鹿泉区宜安中学化学兴趣小组同学为了测 定某石灰石矿中碳酸钙的质量分数.进行了如下实验:往盛 有11g石灰石样品的烧杯中,加入足量稀盐酸后,用电子天平称量反应前后烧杯的质量(如图所示).求:
石家庄市鹿泉区宜安中学化学兴趣小组同学为了测 定某石灰石矿中碳酸钙的质量分数.进行了如下实验:往盛 有11g石灰石样品的烧杯中,加入足量稀盐酸后,用电子天平称量反应前后烧杯的质量(如图所示).求: