题目内容
4.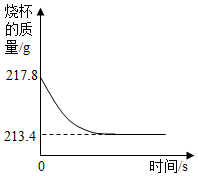 石家庄市鹿泉区宜安中学化学兴趣小组同学为了测 定某石灰石矿中碳酸钙的质量分数.进行了如下实验:往盛 有11g石灰石样品的烧杯中,加入足量稀盐酸后,用电子天平称量反应前后烧杯的质量(如图所示).求:
石家庄市鹿泉区宜安中学化学兴趣小组同学为了测 定某石灰石矿中碳酸钙的质量分数.进行了如下实验:往盛 有11g石灰石样品的烧杯中,加入足量稀盐酸后,用电子天平称量反应前后烧杯的质量(如图所示).求:(1)反应生成二氧化碳的质量是4.4g.
(2)石灰石矿中碳酸钙的质量分数(矿石中杂质不与盐酸反应,反应中水蒸气的挥发忽略不计.计算结果保留1位小 数.)
分析 (1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;
(2)根据化学方程式由二氧化碳的质量可以计算出碳酸钙的质量,进而计算出石灰石矿中碳酸钙的质量分数.
解答 解:(1)根据质量守恒定律,二氧化碳的质量为:217.8g-213.4g=4.4g;故填:4.4;
(2)解:设样品中碳酸钙的质量是x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
X 4.4g
$\frac{100}{44}$=$\frac{x}{4.4g}$
X═10g
石灰石矿中碳酸钙的质量分数是$\frac{10g}{11g}$×100%≈90.9%
答:石灰石矿中碳酸钙的质量分数是90.9%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
15.下列做法不是利用中和反应原理的是( )
| A. | 用熟石灰改良酸性土壤 | B. | 用含氢氧化镁的药物治疗胃酸过多 | ||
| C. | 用纯碱溶液除去发面中过多的乳酸 | D. | 用氨水(NH3•H2O)处理废水中的硫酸 |
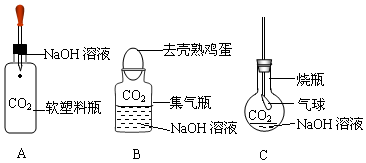
12. 探究小组用如图装置进行实验.胶头滴管和集气瓶中分别盛装不同物质.挤压胶头滴管,向集气瓶中滴加适量液体后,能观察到气球变大的组合是( )
探究小组用如图装置进行实验.胶头滴管和集气瓶中分别盛装不同物质.挤压胶头滴管,向集气瓶中滴加适量液体后,能观察到气球变大的组合是( )
 探究小组用如图装置进行实验.胶头滴管和集气瓶中分别盛装不同物质.挤压胶头滴管,向集气瓶中滴加适量液体后,能观察到气球变大的组合是( )
探究小组用如图装置进行实验.胶头滴管和集气瓶中分别盛装不同物质.挤压胶头滴管,向集气瓶中滴加适量液体后,能观察到气球变大的组合是( )| A. | 稀盐酸和石灰石 | B. | 水和氧化钙 | C. | 水和硝酸铵 | D. | 水和氢氧化钠 |
9.化学与日常生活、工农业生产密切相关,下列说法中不正确的是( )
| A. | 用含有碳酸氢钠的发酵粉培制糕点 | B. | 工业上用熟石灰处理硫酸厂的污水 | ||
| C. | 医疗上用纯酒精作消毒剂 | D. | 生活中用含有NaOH的清洁剂去油污 |
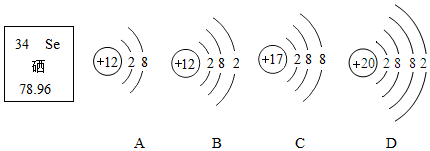
16.下列有关SO2的说法中,错误的是( )
| A. | 表示一个二氧化硫分子 | |
| B. | 由硫和氧气两种物质组成 | |
| C. | 物质名称是“二氧化硫” | |
| D. | 每个分子是由两个氧原子和一个硫原子构成的 |
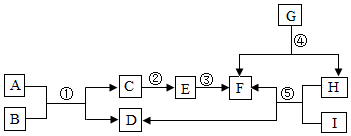 A~I是目前我们已学的常见物质,它们的相互转化关系如图所示(有反应条件、反应物和生成物未给出).已知A、D是组成元素相同的无色气体;G、F组成元素也相同,在常温下都是液体,E是最理想能源物质;C是世界上产量最高的金属.
A~I是目前我们已学的常见物质,它们的相互转化关系如图所示(有反应条件、反应物和生成物未给出).已知A、D是组成元素相同的无色气体;G、F组成元素也相同,在常温下都是液体,E是最理想能源物质;C是世界上产量最高的金属.