题目内容
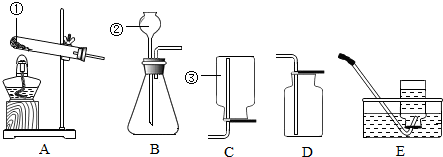
7.根据下列装置图填空:
(1)写出编号①、②仪器的名称:①长颈漏斗;②酒精灯.
(2)实验室制取二氧化碳的发生装置应选用A(填序号,下同),收集装置应选用D;在实验室用加热高锰酸钾制取氧气的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,发生装置应选用B,收集装置可选用D或E.
(3)由此我们得到启示:实验室选择气体发生装置时,应考虑反应物状态和反应条件;选择气体收集装置时,应考虑密度和溶解性.
分析 (1)根据实验装置图中仪器图,辨认常用仪器,并写出仪器的名称;
(2)装置A为用于固体加热类反应的发生装置,装置B适用于固体与液体在常温下反应制取气体类反应的发生装置;装置C为排水法收集气体,适用于不溶于水的气体的收集;装置D,由于导管未伸入集气瓶底部,是个错误的收集装置;装置E为向上排气法收集装置,用于密度大于空气的气体的收集;
(3)反应的原理决定了反应发生装置的选取,而气体的性质密度和溶解性则是决定气体收集装置的主要因素.
解答 解:(1)仪器①为长颈漏斗,仪器②为酒精灯,故答案为:长颈漏斗;酒精灯;
(2)实验室制取二氧化碳使用块状固体石灰石和液体稀盐酸在常温下反应,属于固体与液体常温下发生反应制取气体类型,应选的发生装置为A;二氧化碳密度比空气大且能溶于水,因此收集二氧化碳只能用装置D向上排空气法收集;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,故其化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;实验室用加热高锰酸钾的方法制取氧气,属于固体加热制取气体的类型,应选B装置作为发生装置;氧气密度大于空气,不易溶于水,可用向上排空气法装置D或排水法装置E进行收集,故答案为:A;D;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;B;D或E;
(3)实验室制取气体时发生装置的选用取决于反应所使用药品的状态及反应所需要的条件;而收集气体时,主要根据气体的密度与溶解性进行收集装置的选择,故答案为:反应物状态;反应条件;密度;溶解性.
故答案为:
(1)长颈漏斗;酒精灯;(2)A;D;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;B;D或E;(3)反应物状态;反应条件;密度;溶解性.
点评 本题需要考虑实验室制取气体时的发生装置主要分为:固体与液体常温下反应类与固体加热下反应类两种;收集气体则根据气体的密度和溶解性可采取向上或向下排气法收集、排水法收集三种.

 阅读快车系列答案
阅读快车系列答案| A. |  塑料水盆 | B. |  不锈钢龙头 | C. |  木桶 | D. |  纯棉毛巾 |
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl |
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.利用沉淀物质量计算Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%.(大于、小于、等于)
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).

(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D.
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿.根据质量守恒定律,装置C(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果偏大(选填“偏大”或“偏小”).
| A. | 水结冰 | B. | 水电解生成氢气和氧气 | ||
| C. | 水蒸发 | D. | 把铁块粉碎 |
| A. | 大量植树造林,禁止乱砍滥伐 | B. | 尽量乘坐公交车或自行车出行 | ||
| C. | 提倡使用节能技术和节能产品 | D. | 大量使用化石燃料 |