题目内容
欲将含有盐酸的CaCl2溶液中和至中性,在不加指示剂的条件下,可选用的试剂是( )
| A、石灰石粉末 | B、石灰水 |
| C、碳酸钠溶液 | D、生石灰粉末 |
考点:酸的化学性质
专题:常见的酸 酸的通性
分析:氯化钙溶液因含有盐酸显酸性要变为中性,即是要除去其中的盐酸.注意过程中不能增加其他可溶性的杂质.
解答:解:A、石灰石的主要成分是碳酸钙能与盐酸反应生成氯化钙,且碳酸钙不溶于水,可加入过量的石灰石粉末将盐酸除去.故选;
B、石灰水的主要成分是氢氧化钙,能与盐酸反应生成氯化钙,反应时无明显现象不好控制加入的量.故不选;
C、碳酸钠能与盐酸反应生成氯化钠虽能除去盐酸但却增加了新的杂质.故不选.
D、生石灰的主要成分是氧化钙,能与水反应生成氢氧化钙,可以盐酸反应生成氯化钙,反应时无明显现象,不好控制加入的量.故不选;
故选A.
B、石灰水的主要成分是氢氧化钙,能与盐酸反应生成氯化钙,反应时无明显现象不好控制加入的量.故不选;
C、碳酸钠能与盐酸反应生成氯化钠虽能除去盐酸但却增加了新的杂质.故不选.
D、生石灰的主要成分是氧化钙,能与水反应生成氢氧化钙,可以盐酸反应生成氯化钙,反应时无明显现象,不好控制加入的量.故不选;
故选A.
点评:解答除杂相关问题时要把握如下原则:①选用的试剂要能将杂质除去但不能与要保留的物质反应②在除杂的同时不能增加新的杂质.一般的方法是将杂质转化为要保留的物质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
为完全中和某一盐酸溶液,需用10克质量分数为10%的NaOH溶液,如果改用10克质量分数为10%的KOH溶液,反应后的pH值( )
| A、大于7 | B、小于7 |
| C、等于7 | D、无法判断 |
用扇子一扇,燃着的蜡烛立即熄灭,原因是( )
| A、供给的氧气减少 |
| B、供给的空气增加 |
| C、使蜡烛的着火点降低 |
| D、将温度降低至蜡烛的着火点以下 |
金刚石、石墨和C60的化学性质相似,物理性质却有很大差异.其原因是( )
| A、构成它们的原子大小不同 |
| B、构成它们的原子数目不同 |
| C、金刚石、石墨和C60里碳原子的排列方式不同 |
| D、金刚石、石墨和C60由不同种原子构成 |
 氢原子
氢原子 氧原子,比较分析回答问题:
氧原子,比较分析回答问题:
 某同学欲探究市售“双钙防蛀”牙膏、“皓清”牙膏和牙粉的主要成分.
某同学欲探究市售“双钙防蛀”牙膏、“皓清”牙膏和牙粉的主要成分.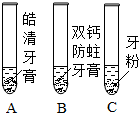

 2014年4月26日据央视调查报道(黑金之祸).黑龙江省鸡西市鸡东县饮用水铅超标700倍,汞超标9倍.而这一切都是石墨过度开采,加工过程导致环境污染.石墨是用于手机电池与电动车电池加工的主要材料.2010年石墨每吨是2000元而2014年的石墨价格是每吨6000元.巨大的“利益”就是导火索.
2014年4月26日据央视调查报道(黑金之祸).黑龙江省鸡西市鸡东县饮用水铅超标700倍,汞超标9倍.而这一切都是石墨过度开采,加工过程导致环境污染.石墨是用于手机电池与电动车电池加工的主要材料.2010年石墨每吨是2000元而2014年的石墨价格是每吨6000元.巨大的“利益”就是导火索.