题目内容
12.化学与我们生活、学习关系密切.(1)在由碳元素形成的各种单质中,可用于切割玻璃和大理石的是金刚石,冰箱除味剂的利用活性炭的吸附性,干电池中碳棒是利用石墨的导电性.
(2)“84”消毒液可用于灾区防疫,其主要成分是次氯酸钠(NaClO),制取它的化学方程式为2NaOH+CL2═NaClO+X+H2O,则X的化学式为NaCl,求出NaClO中氯元素化合价并在该化学式中表示出来Na$\stackrel{+1}{Cl}$O.
(3)在实验室里可加热高锰酸钾固体制氧气,写出该反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应的基本反应类型为分解反应.
(4)固体MgH2是氢能源汽车的供能剂,MgH2可以和水反应生成氢氧化镁,同时释放出氢气,该反应的化学方程式为MgH2+2H2O=Mg(OH)2+2H2↑.
分析 (1)根据常见的碳的单质的性质与用途来分析;
(2)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
根据在化合物中正负化合价代数和为零,结合NaClO的化学式进行解答即可;
(3)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型;
(4)根据反应的原理以及化学方程式的写法来分析.
解答 解:(1)金刚石是硬度最大的矿物,可用来切割玻璃和大理石;活性炭具有很好的吸附性,可用啦做除味剂;石墨具有导电性,可用来作电极;故填:金刚石;吸附;导电;
(2)根据反应的化学方程式2NaOH+Cl2═NaClO+X+H2O,反应物中钠、氢、氧、氯原子个数分别为2、2、2、2,反应后的生成物中钠、氢、氯、氧原子个数分别为1、2、1、2,根据反应前后原子种类、数目不变,则X分子中含有1个氯原子和1个钠原子,则物质X的化学式为NaCl.
钠元素显+1价,氧元素显-2价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)=0,则x=+1价.
故填:NaCl;Na$\stackrel{+1}{Cl}$O;
(3)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;该反应符合“一变多”的特征,属于分解反应.故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;分解反应;
(4)氢化镁MgH2可以和水反应生成氢氧化镁和氢气,该反应的化学方程式是MgH2+2H2O=Mg(OH)2+2H2↑.故填:MgH2+2H2O=Mg(OH)2+2H2↑.
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.

| A. | 实验剩余的药品应放回原试剂瓶 | |
| B. | 给烧杯加热时,要垫上石棉网 | |
| C. | 加热试管中的固体时试管口略向上倾斜 | |
| D. | 把块状固体投入直立的试管中 |
 9月16日我校举办了声势浩大的秋季运动会,在欢乐轻松的氛围中发扬体育精神.田径比赛时发令员使用的发令枪如图所示,下列有关说法不正确的是( )
9月16日我校举办了声势浩大的秋季运动会,在欢乐轻松的氛围中发扬体育精神.田径比赛时发令员使用的发令枪如图所示,下列有关说法不正确的是( )| A. | 发令枪使用的无缝钢管是纯铁制作 | |
| B. | 计时员看到发令枪冒烟开始计时 | |
| C. | 发令枪子弹弹壳采用的黄铜是铜锌合金 | |
| D. | 使用后的发令枪要及时清理擦净污垢避免锈蚀 |
| A. | 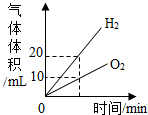 将水通电一段时间,相同状况下产生气体的体积变化 | |
| B. | 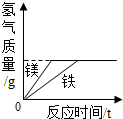 常温下,足量的镁、铁分别同时放入少量等质量、等浓度的稀盐酸中 | |
| C. |  向一定量二氧化锰固体中加入一定量过氧化氢溶液 | |
| D. |  工业上煅烧石灰石制取二氧化碳 |
| A. | l:4 | B. | 4:l | C. | 3:8 | D. | 8:3 |
| A. | 修建通屯水泥路 | B. | 养花种果树 | ||
| C. | 派保洁员清扫路面垃圾 | D. | 污水直接通入到河流中 |

 a、b、c三种物质的溶解度曲线按如图所示,据图回答:
a、b、c三种物质的溶解度曲线按如图所示,据图回答: