题目内容
10.钛(Ti)被称为继铁、铝之后的第三金属.如图所示,将钛厂、氯碱厂和甲醇(CH4O)厂组成产业链可以大大提高资源利用率,减少环境污染.

(1)电解食盐水反应的化学方程式为2H2O+2NaCl═2NaOH+H2↑+Cl2↑.
(2)由四氯化钛和镁制取钛的反应,基本反应类型为置换反应.该过程中,氩气的作用是隔绝空气,防止镁与空气中的成分(O2、N2等)反应.
分析 (1)电解食盐水生成氢氧化钠、氢气和氯气,写出反应的化学方程式即可.
(2)由四氯化钛和镁制取钛,生成钛和氯化镁,镁能与空气中的氧气、氮气等反应,进行分析解答.
解答 解:(1)电解食盐水生成氢氧化钠、氢气和氯气,反应的化学方程式为:2H2O+2NaCl═2NaOH+H2↑+Cl2↑.
(2)四氯化钛和镁制取钛,生成钛和氯化镁,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
镁能与空气中的氧气、氮气等反应,该过程中,氩气的作用是隔绝空气,防止镁与空气中的成分(O2、N2等)反应.
故答案为:(1)2H2O+2NaCl═2NaOH+H2↑+Cl2↑;
(2)置换反应;隔绝空气,防止镁与空气中的成分(O2、N2等)反应.
点评 本题难度不大,理解钛厂、氯碱厂和甲醇厂组成产业链的流程,掌握置换反应的特征、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
相关题目
4.我国女科学家屠呦呦发现了青蒿素,一种用于治疗疟疾的药物,获得诺贝尔生理学或医学奖.关于青蒿素[C15H22O5]说法正确的是( )
| A. | 青蒿素属于氧化物 | B. | 青蒿素的相对分子质量是282g | ||
| C. | 青蒿素碳元素的质量分数最高 | D. | 青蒿素有42个原子 |
5.某课外小组进行了如下实验.
(1)实验Ⅰ中反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(2)实验Ⅱ的目的是比较高锰酸钾和碘在汽油中的溶解情况.
(3)实验Ⅲ,倒流入集气瓶中的水小于瓶中气体体积的$\frac{1}{5}$,原因是红磷不足或气密性不好.
(4)实验Ⅳ中,观察到U型管左侧液面下降的原因是生石灰遇水放热,使得大试管中的气体受热膨胀,压强增大.
| 序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 实验 | 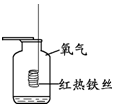 | 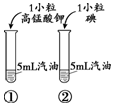 | 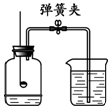 | 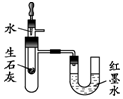 |
| 操作及现象 | 剧烈燃烧,火星四射,生成黑色固体,放热 | 试管①中固体几乎不溶解;试管②中固体溶解,形成紫红色溶液 | 红磷燃烧产生白烟,熄灭后冷却至室温,打开弹簧夹,水倒流入集气瓶中 | 将胶头滴管中的水滴入试管中,一段时间后,观察到U型管左侧液面下降 |
(2)实验Ⅱ的目的是比较高锰酸钾和碘在汽油中的溶解情况.
(3)实验Ⅲ,倒流入集气瓶中的水小于瓶中气体体积的$\frac{1}{5}$,原因是红磷不足或气密性不好.
(4)实验Ⅳ中,观察到U型管左侧液面下降的原因是生石灰遇水放热,使得大试管中的气体受热膨胀,压强增大.
2.下列说法中,正确的是( )
| A. | 家用电器着火,立即用水泼灭 | |
| B. | 公路上的积雪可以用氯化钠来消除 | |
| C. | 发令枪中红磷燃烧时产生大量白雾 | |
| D. | 生铁和钢都是铁合金,在用途上没有区别 |
19.蚊子、蜂、蚂蚁等昆虫叮咬人后,会向人注入一种叫蚁酸(甲酸)的物质,使皮肤红肿疼痛,要消除肿痛,可涂下列物质中的( )
| A. | 硼酸 | B. | 氢氧化钠溶液 | C. | 肥皂水 | D. | 食用醋 |
20.下列关于溶液的说法正确的是( )
| A. | 具有均一性、稳定性的液体一定是溶液 | |
| B. | 配制溶液时,搅拌可以增大固体物质的溶解度 | |
| C. | 饱和溶液一定比不饱和溶液的浓度大 | |
| D. | 析出晶体后的溶液,溶质质量分数不一定减小 |
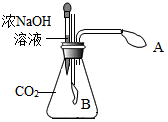 二氧化碳与氢氧化钠溶液作用没有明显的现象,某同学设计了图所示的实验装置(A、B是气球)探究二氧化碳与氢氧化钠溶液的反应.
二氧化碳与氢氧化钠溶液作用没有明显的现象,某同学设计了图所示的实验装置(A、B是气球)探究二氧化碳与氢氧化钠溶液的反应. 淮南珍珠泉因“泉水涌出珠”而得名,其泉水中冒出珍珠似的气泡,气泡内气体是沼气(主要成分为CH4).为了测定该沼气中含有CH4的质量分数,在密闭容器中充分燃烧20g沼气(假设杂质不可燃)与一定量氧气恰好完全反应,反应前后容器内质量如图,请计算
淮南珍珠泉因“泉水涌出珠”而得名,其泉水中冒出珍珠似的气泡,气泡内气体是沼气(主要成分为CH4).为了测定该沼气中含有CH4的质量分数,在密闭容器中充分燃烧20g沼气(假设杂质不可燃)与一定量氧气恰好完全反应,反应前后容器内质量如图,请计算