题目内容
16.下列物质中,属于混合物的是①③⑤⑨⑩;属于纯净物的是②④⑥⑦⑧.(填序号)①河水; ②五氧化二磷; ③纯净的空气;④二氧化碳; ⑤稀有气体; ⑥四氧化三铁; ⑦硫粉;⑧冰水混合物;⑨加热高锰酸钾后的剩余物; ⑩医用酒精.
分析 纯净物是由一种物质组成的物质,混合物是由多种物质组成的物质.据此根据物质的组成方面进行分析、判断.
解答 解:①河水;③纯净的空气; ⑤稀有气体;⑨加热高锰酸钾后的剩余物; ⑩医用酒精等物质中都含有多种物质,都属于混合物;
②五氧化二磷;④二氧化碳; ⑥四氧化三铁;⑦硫粉;⑧冰水混合物等物质都是由一种物质组成的,都属于纯净物.
故填:①③⑤⑨⑩;②④⑥⑦⑧.
点评 解答本题要分析物质是由几种物质组成的,如果只有一种物质组成就属于纯净物.

练习册系列答案
相关题目
6.某同学家新换了淋浴喷头,从说明书上了解到该喷头是铜制镀铬的,他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝铜在金属活动性顺序中的相对位置关系,进行如下探究活动:
【查阅资料】①铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜.②铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
③铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
【回答问题】(1)用砂纸打磨金属片的目的是除去金属表面氧化物.
(2)实验一发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)甲同学提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,你认为不可行(填“可行”或“不可行”).
(4)乙同学认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品应该是A1、CrSO4溶液、Cu.
【归纳】比较金属活动性强弱的方法有:
①通过金属与酸反应判断金属活动性强弱;
②通过金属与盐溶液反应判断金属活动性强弱.
【查阅资料】①铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜.②铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
③铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验 | 实验一 | 实验二 | 实验三 |
| 实验方案 |  | 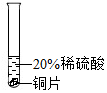 | 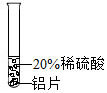 |
| 实验现象 | 铬片表面产生气泡缓慢,溶液变为蓝色 | 无明显现象 | 铝片表面产生气泡较快 |
| 结论 | 铬能与稀硫酸反应,反应速率较慢 | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是Al>Cr>Cu. | |||
(2)实验一发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)甲同学提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,你认为不可行(填“可行”或“不可行”).
(4)乙同学认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品应该是A1、CrSO4溶液、Cu.
【归纳】比较金属活动性强弱的方法有:
①通过金属与酸反应判断金属活动性强弱;
②通过金属与盐溶液反应判断金属活动性强弱.
7.规范的操作是实验成功的前提.实验操作正确的是( )
| A. | 检查装置气密性时,先用手握住试管,再将导管放入水中 | |
| B. | 取少量液体试剂时,滴管伸入试剂瓶内液体中,挤压胶头吸液 | |
| C. | 用试管夹夹持试管给液体加热时,需要移动试管,以防受热不均和液体冲出 | |
| D. | 实验结束后,剩余的试剂都应放回原试剂瓶 |
4.在“空气中氧气含量的测定”实验探究中,
①甲同学设计了如图1的实验方案:在集气瓶内放足量红磷,塞紧橡皮塞,用放大镜聚集太阳光来引燃红磷,待红磷火焰熄灭且集气瓶冷却至室温后,打开止水夹.如果实验成功,那实验过程中观察到的主要现象有产生大量白烟、水倒吸入集气瓶约占$\frac{1}{5}$体积.

②乙同学设计了如图2的实验方案:将足量镁粉点燃后放入钟罩装置进行实验,写出镁粉与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.燃烧完毕冷却后水几乎占满整个钟罩,已知镁是一种很活泼的金属,请推测产生这一现象的可能原因镁不仅和氧气反应,还与氮气发生反应.如果将图2中镁粉换成碳粉进行相同实验,则不能 (能或不能)用来测定空气中氧气的含量.
③丙同学设计了如图3的实验方案:反应容器是由两个针筒和中间的玻璃管组成的密闭系统,容器内留有30mL空气.加热等铜丝的温度升高后,交替缓缓推动两个注射器活塞,观察到亮红色的铜丝表面覆盖着一层黑色物质(反应方程式:2Cu+O2 $\stackrel{△}{→}$ 2CuO),实验数据记录如下:
Ⅰ.反应后容器内气体体积X理论上为24mL.
Ⅱ.如果反应结束后测得容器内气体体积为28mL,假设装置气密性完好,那造成实验有误差的原因可能是铜丝过少 (试举一个即可).
④十八世纪法国化学家拉瓦锡为了研究空气的组成设计的实验如图4,实验原理是汞与氧气在加热条件下会反应生成红色的氧化汞粉末.当年拉瓦锡在观察到汞表面浮起红色渣滓后,还继续加热了12天才停止实验,他这样做的理由是为了保证把装置内的氧气全部反应完.
①甲同学设计了如图1的实验方案:在集气瓶内放足量红磷,塞紧橡皮塞,用放大镜聚集太阳光来引燃红磷,待红磷火焰熄灭且集气瓶冷却至室温后,打开止水夹.如果实验成功,那实验过程中观察到的主要现象有产生大量白烟、水倒吸入集气瓶约占$\frac{1}{5}$体积.

②乙同学设计了如图2的实验方案:将足量镁粉点燃后放入钟罩装置进行实验,写出镁粉与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.燃烧完毕冷却后水几乎占满整个钟罩,已知镁是一种很活泼的金属,请推测产生这一现象的可能原因镁不仅和氧气反应,还与氮气发生反应.如果将图2中镁粉换成碳粉进行相同实验,则不能 (能或不能)用来测定空气中氧气的含量.
③丙同学设计了如图3的实验方案:反应容器是由两个针筒和中间的玻璃管组成的密闭系统,容器内留有30mL空气.加热等铜丝的温度升高后,交替缓缓推动两个注射器活塞,观察到亮红色的铜丝表面覆盖着一层黑色物质(反应方程式:2Cu+O2 $\stackrel{△}{→}$ 2CuO),实验数据记录如下:
| 反应前容器内空气体积 | 反应后容器内气体体积 |
| 30mL | X mL |
Ⅱ.如果反应结束后测得容器内气体体积为28mL,假设装置气密性完好,那造成实验有误差的原因可能是铜丝过少 (试举一个即可).
④十八世纪法国化学家拉瓦锡为了研究空气的组成设计的实验如图4,实验原理是汞与氧气在加热条件下会反应生成红色的氧化汞粉末.当年拉瓦锡在观察到汞表面浮起红色渣滓后,还继续加热了12天才停止实验,他这样做的理由是为了保证把装置内的氧气全部反应完.
11.某同学用托盘天平称量5.6克药品时,结果发现指针向左偏,接下来怎么样使天平平衡( )
| A. | 加砝码 | B. | 移动游码 | C. | 调节平衡螺母 | D. | 减少药品 |
8.在日常生活中,同学们常常见到下列一些变化,其中属于物理变化的是( )
| A. | 食物腐败 | B. | 菜刀生锈 | C. | 碘受热升华 | D. | 红磷燃烧 |
6.元素R的化合价只有1种,其硫酸盐的化学式为R2(SO4)3,下列化学式错误的是( )
| A. | R(NO3)3 | B. | R(OH)2 | C. | R2O3 | D. | RCl3 |

 明矾是一种白色晶体(见如图),可用于炸制油条、自来水厂净水等,其化学式为KAl(SO4)2•12H2O,试根据明矾的化学式完成下列各题.
明矾是一种白色晶体(见如图),可用于炸制油条、自来水厂净水等,其化学式为KAl(SO4)2•12H2O,试根据明矾的化学式完成下列各题.