题目内容
6.某同学家新换了淋浴喷头,从说明书上了解到该喷头是铜制镀铬的,他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝铜在金属活动性顺序中的相对位置关系,进行如下探究活动:【查阅资料】①铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜.②铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
③铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验 | 实验一 | 实验二 | 实验三 |
| 实验方案 |  | 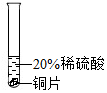 | 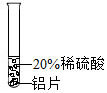 |
| 实验现象 | 铬片表面产生气泡缓慢,溶液变为蓝色 | 无明显现象 | 铝片表面产生气泡较快 |
| 结论 | 铬能与稀硫酸反应,反应速率较慢 | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是Al>Cr>Cu. | |||
(2)实验一发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)甲同学提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,你认为不可行(填“可行”或“不可行”).
(4)乙同学认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品应该是A1、CrSO4溶液、Cu.
【归纳】比较金属活动性强弱的方法有:
①通过金属与酸反应判断金属活动性强弱;
②通过金属与盐溶液反应判断金属活动性强弱.
分析 本题中,题目首先给出了三个实验探究方案,可以根据金属与酸或盐的反应规律,就能够解决.
回答问题:(1)砂纸打磨是为了除去金属表面的氧化物或污染物;
(2)根据铬与稀硫酸反应生成硫酸铬和氢气书写;
(3)铬和铝都能和硫酸铜反应,不能检验铬和铝的活动性;
(4)本题开放性比较强,答案不唯一,可以采取“三取中”的检验思路选用Al、CrSO4溶液、Cu,也可以用Al2(SO4)3溶液、Cr、CuSO4溶液,完成活动性验证.
归纳:通过金属和酸的反应现象判断金属的活动性,还可以根据金属和盐溶液的反应判断金属的活动性.
解答 解:根据题设中的实验现象:铬片表面产生气泡缓慢,铜片无明显现象,铝片表面产生气泡较快;可判断:铝能与稀硫酸发生反应,反应速率较快;铬能与稀硫酸发生反应,反应速率缓慢;铜不能与稀硫酸发生反应,则三种金属在金属活动性顺序中的相对位置关系是:Al Cr Cu(或“②”);
回答问题:
(1)砂纸打磨是为了除去金属表面氧化物;
(2)由资料可知,铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液,反应的化学方程式为:Cr+H2SO4=CrSO4+H2↑;
(3)铬和铝都能和硫酸铜反应,不能检验铬和铝的活动性;
(4)利用“三取中”的实验方法,可以用Al、CrSO4溶液、Cu;也可以用Al2(SO4)3溶液、Cr、CuSO4溶液.
归纳:通过金属和酸的反应现象判断金属的活动性,还可以根据金属和盐溶液的反应判断金属的活动性.
故答案为:结论:Al>Cr>Cu;
回答问题:(1)除去金属表面氧化物;
(2)Cr+H2SO4=CrSO4+H2↑;
(3)不可行;
(4)A1、CrSO4溶液、Cu;
归纳:①通过金属与酸反应判断金属活动性强弱.
点评 验证三种金属活动性强弱关系时,通常采取“三取中”即:取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案| A. | 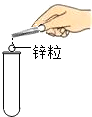 取用锌粒 | B. |  过滤泥水 | C. | 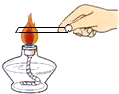 加热铜片 | D. | 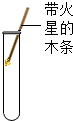 检验氧气 |
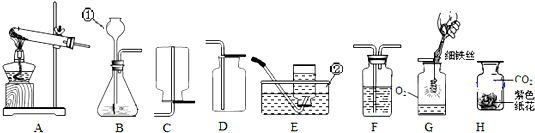
 如图,将一支盛有CO2的试管倒立砸一个装满水的烧杯中看到试管内液面上升一段水柱;原因是二氧化碳能与水反应生成碳酸,使试管内气体压强减小,在外界大气压的作用下液体被压入试管内,所以试管内液面上升
如图,将一支盛有CO2的试管倒立砸一个装满水的烧杯中看到试管内液面上升一段水柱;原因是二氧化碳能与水反应生成碳酸,使试管内气体压强减小,在外界大气压的作用下液体被压入试管内,所以试管内液面上升