题目内容
2.下列计算或结果正确的是( )| A. | Ca(OH)2的相对分子质量=40+16+1×2=58 | |
| B. | SO2中硫元素与氧元素的质量比是2:1 | |
| C. | CO2中氧元素的质量分数 60% | |
| D. | 54g水中含有氢元素6g |
分析 A、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分判断.
C、根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析判断.
D、根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析判断.
解答 解:A、Ca(OH)2的相对分子质量=(40+16+1)×2=74,故选项说法错误.
B、SO2中硫元素与氧元素的质量比是32:(16×2)=1:1,故选项说法错误.
C、CO2中氧元素的质量分数为$\frac{16×2}{12+16×2}×$100%≈72.7%,故选项说法错误.
D、54g水中含有氢元素的质量为54g×$\frac{1×2}{1×2+16}×$100%=6g,故选项说法正确.
故选:D.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
11. 某校化学兴趣小组在探究铁的锈蚀条件后发现该实验耗时较长.为解决此问题,在教师的指导下进行了更深入的探究.探究过程如下:
某校化学兴趣小组在探究铁的锈蚀条件后发现该实验耗时较长.为解决此问题,在教师的指导下进行了更深入的探究.探究过程如下:
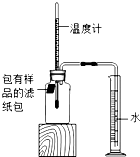
如图所示(该装置气密性良好),室温时,将包有样品的滤纸包用大头针固定在橡皮塞上,迅速塞紧橡皮塞.已知,此集气瓶净容积为146mL.一段时间后,观察到量筒内水沿导管进入集气瓶.当温度恢复至室温,且量筒内水面高度不再发生变化时读数(此时瓶内氧气含量近似为零).
记录起始和最终量筒的读数以及所需时间如下表.
下列说法中不正确的是( )
(1)温度计示数一直增大;
(2)样品中有红色固体生成;
(3)该实验说明铁生锈速率与氯化钠有关;
(4)该实验测得O2体积分数为20.5%;
(5)该实验能探究木炭加快铁锈蚀速率.
 某校化学兴趣小组在探究铁的锈蚀条件后发现该实验耗时较长.为解决此问题,在教师的指导下进行了更深入的探究.探究过程如下:
某校化学兴趣小组在探究铁的锈蚀条件后发现该实验耗时较长.为解决此问题,在教师的指导下进行了更深入的探究.探究过程如下:如图所示(该装置气密性良好),室温时,将包有样品的滤纸包用大头针固定在橡皮塞上,迅速塞紧橡皮塞.已知,此集气瓶净容积为146mL.一段时间后,观察到量筒内水沿导管进入集气瓶.当温度恢复至室温,且量筒内水面高度不再发生变化时读数(此时瓶内氧气含量近似为零).
记录起始和最终量筒的读数以及所需时间如下表.
| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| Ⅰ | 1g铁粉、0.2g木炭粉和10滴水 | 100 | 70 | 约120 |
| Ⅱ | lg铁粉、0.2g木炭粉、10滴水和少量氯化钠 | 100 | 70 | 约70 |
(1)温度计示数一直增大;
(2)样品中有红色固体生成;
(3)该实验说明铁生锈速率与氯化钠有关;
(4)该实验测得O2体积分数为20.5%;
(5)该实验能探究木炭加快铁锈蚀速率.
| A. | (3)(4) | B. | (1)(3) | C. | (1)(5) | D. | (4)(5) |
12.下列电离方程式正确的是( )
| A. | H2SO4═H2++SO42- | B. | MgSO4═Mg2++SO42- | ||
| C. | Ca(OH)2=Ca2++OH2- | D. | BaCl2=Ba2++Cl2- |
14.2011年3月,日本福岛第一核电站发生核辐射泄漏,日本政府向福岛核电站附近居民发放碘片(I-127),以降低放射性碘对人体的伤害.已知核辐射中放射性碘(I-131)的核电荷数是53,则下列说法不正确的是( )
| A. | 核裂变是一种化学变化 | |
| B. | 碘I-127原子和碘I-131原子属于同种元素 | |
| C. | 核能的利用证实了原子的可分性 | |
| D. | 碘I-131原子的中子数是78 |