题目内容
硫酸(H2SO4)常用作气体干燥剂.计算
(1)硫酸中氢、氧、硫三种元素的质量比; ;
(2)硫酸中氧元素的质量分数.列式并计算
(3)硫酸的相对分子量 ;
(4)100g硫酸中含有氧元素的质量是 g;
(5)H2SO4中S元素的化合价是 .
(1)硫酸中氢、氧、硫三种元素的质量比;
(2)硫酸中氧元素的质量分数.列式并计算
(3)硫酸的相对分子量
(4)100g硫酸中含有氧元素的质量是
(5)H2SO4中S元素的化合价是
考点:元素质量比的计算,有关元素化合价的计算,相对分子质量的概念及其计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中元素的质量分数=
×100%,进行分析解答.
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(4)根据化合物中元素的质量分数=
×100%,进行分析解答.
(5)根据化合物中化合价的原则,进行分析解答.
(2)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(4)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(5)根据化合物中化合价的原则,进行分析解答.
解答:解:
(1)硫酸中氢、氧与硫元素的质量比是(1×2):(16×4):32=1:32:16.
(2)100g硫酸中含有氧元素的质量分数是
×100%≈65.3%
(3)硫酸的相对分子质量1×2+32+16×4=98.
(4)100g硫酸中含有氧元素的质量是100g×
×100%≈65.3g.
(5)设H2SO4中S元素的化合价为x,则(+1)×2+x+(-2)×4=0,解得x=+6.
故答案为:
(1)1:32:16;(2)65.3%;(3)98;(4)65.3g;(5)+6.
(1)硫酸中氢、氧与硫元素的质量比是(1×2):(16×4):32=1:32:16.
(2)100g硫酸中含有氧元素的质量分数是
| 16×4 |
| 98 |
(3)硫酸的相对分子质量1×2+32+16×4=98.
(4)100g硫酸中含有氧元素的质量是100g×
| 16×4 |
| 98 |
(5)设H2SO4中S元素的化合价为x,则(+1)×2+x+(-2)×4=0,解得x=+6.
故答案为:
(1)1:32:16;(2)65.3%;(3)98;(4)65.3g;(5)+6.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 北京时间2011年3月11日,日本附近海域发生了9.0级地震,地震引发了海啸.
北京时间2011年3月11日,日本附近海域发生了9.0级地震,地震引发了海啸.
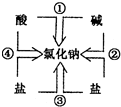
 如图是书中说明氯化钠在生活中的用途的图片.
如图是书中说明氯化钠在生活中的用途的图片.