题目内容
 北京时间2011年3月11日,日本附近海域发生了9.0级地震,地震引发了海啸.
北京时间2011年3月11日,日本附近海域发生了9.0级地震,地震引发了海啸.Ⅰ.地震及其次生灾害(如火灾等)使众多灾民食物和饮用水短缺.
(1)地震时,家庭防止次生火灾的措施:一是在大震来临前的小晃动时及大晃动暂停时,应立即关闭正在使用的热水器、煤气灶等;二是在刚失火一二分钟内,用水或灭火器扑灭火苗.其中关闭煤气灶、用水灭火的原理分别是
(2)海啸发生后,饮用水匮乏.若灾民想通过净化附近的河水(假设未受海水及核泄漏污染)来饮用,请你为他们提供一些可行的净水方法
(3)地震发生后,地方政府一天给每个灾民配发一瓶矿泉水、2个饭团(若饭团的成分为大米、紫菜、胡萝卜、白糖和少量食盐),则从营养均衡角度看,配发的食品中缺乏的营养素是
Ⅱ.受地震及海啸影响,日本福岛核电站发生了爆炸、核泄漏.因讹传“核泄漏污染了海盐”和“吃碘盐能防核辐射”,我国部分地区发生了食盐抢购风潮,一时间谣“盐”四起.
(4)食盐的主要成分是氯化钠,氯化钠是由
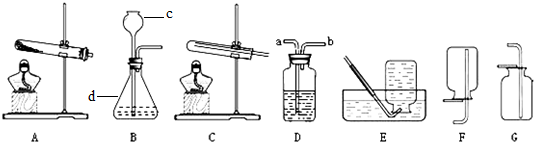
(5)我省的平顶山叶县被誉为“中国岩盐之都”,氯化钠蕴藏量够全国人民吃上几百年,其提纯工艺与实验室粗盐提纯很相似.在做粗盐提纯实验时,多次用到了玻璃棒,其作用有哪些?(至少2条)
(6)岩盐(或称井盐)通常是以“卤水”的形式被抽提出来的.某探究小组欲利用反应NaCl+AgNO3=AgCl↓+NaNO3测定条“卤水”中氯化钠的含量:取卤水100g,加入100g硝酸银溶液时,恰好完全反应(假设卤水中其他成分与硝酸银不反应),测得反应后溶液的质量为156.95g,则该卤水中氯化钠的质量分数是多少?
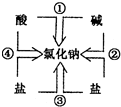
(7)除天然存在外,通过许多化学反应也能得到氯化钠.请根据如图相关信息写出反应②、③的化学方程式.
附:部分物质的溶解性表(20℃)
| OH- | NO
|
Cl- | CO
| |||||
| Na+ | 溶 | 溶 | 溶 | 溶 | ||||
| Ba2+ | 溶 | 溶 | 溶 | 不溶 | ||||
| Ca2+ | 微溶 | 溶 | 溶 | 不溶 | ||||
| Mg2+ | 不溶 | 溶 | 溶 | 微溶 |
考点:灭火的原理和方法,水的净化,有关溶质质量分数的简单计算,氯化钠与粗盐提纯,复分解反应及其发生的条件,分子、原子、离子、元素与物质之间的关系,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算,均衡营养与健康
专题:溶质质量分数与化学方程式相结合的计算,空气与水,常见的盐 化学肥料,化学与生活
分析:(1)灭火的方法有三种:①移走可燃物;②隔绝空气;③降低温度.
(2)净水方法有加明矾使杂质沉降;用活性炭吸附除杂、除异味;通过煮沸来消毒等.
(3)人体所需的六大营养元素有:糖类、蛋白质、脂肪、水、无机盐、维生素;
(4)由金属元素与非金属元素组成的化合物,一般是由离子构成的;
(5)粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程)、转移,其操作顺序为溶解-过滤-蒸发-转移,据此分析玻璃棒的作用,进行解答即可;
(6)根据质量守恒定律求出氯化银的质量,然后根据氯化银的质量求出“卤水”中的氯化钠的质量,然后卤水中氯化钠的质量分数;
(7)根据图示可知②是碱和盐反应生成氯化钠;③是盐和盐反应生成氯化钠的反应,据此写出化学方程式.
(2)净水方法有加明矾使杂质沉降;用活性炭吸附除杂、除异味;通过煮沸来消毒等.
(3)人体所需的六大营养元素有:糖类、蛋白质、脂肪、水、无机盐、维生素;
(4)由金属元素与非金属元素组成的化合物,一般是由离子构成的;
(5)粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程)、转移,其操作顺序为溶解-过滤-蒸发-转移,据此分析玻璃棒的作用,进行解答即可;
(6)根据质量守恒定律求出氯化银的质量,然后根据氯化银的质量求出“卤水”中的氯化钠的质量,然后卤水中氯化钠的质量分数;
(7)根据图示可知②是碱和盐反应生成氯化钠;③是盐和盐反应生成氯化钠的反应,据此写出化学方程式.
解答:解:(1)关闭煤气灶、用水灭火的原理分别是:隔离可燃物;降温至可燃物的着火点以下.
(2)净水方法有加明矾使杂质沉降;用活性炭吸附除杂、除异味;通过煮沸来消毒等.
(3)地震发生后,地方政府一天给每个灾民配发一瓶矿泉水、2个饭团(若饭团的成分为大米、紫菜、胡萝卜、白糖和少量食盐),则从营养均衡角度看,配发的食品中含有水、糖类、维生素、无机盐,但没有脂肪和蛋白质.
(4)食盐的主要成分氯化钠是由氯离子和钠离子构成;
(5)在“粗盐提纯”的实验中,操作步骤为溶解-过滤-蒸发-转移,在溶解、过滤、蒸发、转移操作中都要用到的玻璃仪器是玻璃棒;在溶解操作中玻璃棒的作用是搅拌,加快溶解;在过滤操作中玻璃棒的作用是引流;蒸发时玻璃棒的作用是搅拌,防止局部温度过高,造成液滴飞溅;在转移食盐固体的操作中玻璃棒的作用是转移固体.
(6)生成沉淀的质量是:100g+100g-156.95g=43.05g
设100“卤水”中氯化钠的质量是x
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
x 43.05 g
=
x=11.55g
则该卤水中氯化钠的质量分数是:
×100%=11.55%
答:则该卤水中氯化钠的质量分数是11.55%.
(7)碱与盐反应,生成氯化钠的反应方程式是:2NaOH+CuCl2═2NaCl+Cu(OH)2↓
盐与盐反应,生成氯化钠的反应方程式是:Na2CO3+BaCl2=2NaCl+BaCO3↓.
故答案为:(1)隔离可燃物;降温至可燃物的着火点以下.
(2)加明矾使杂质沉降;用活性炭吸附除杂、除异味;通过煮沸来消毒等.
(3)油脂、蛋白质.
(4)钠离子和氯离子.
(5)加速溶解、引流、防止液体局部过热.
(6)11.55%.
(7)2NaOH+CuCl2═2NaCl+Cu(OH)2↓;Na2CO3+BaCl2=2NaCl+BaCO3↓.
(2)净水方法有加明矾使杂质沉降;用活性炭吸附除杂、除异味;通过煮沸来消毒等.
(3)地震发生后,地方政府一天给每个灾民配发一瓶矿泉水、2个饭团(若饭团的成分为大米、紫菜、胡萝卜、白糖和少量食盐),则从营养均衡角度看,配发的食品中含有水、糖类、维生素、无机盐,但没有脂肪和蛋白质.
(4)食盐的主要成分氯化钠是由氯离子和钠离子构成;
(5)在“粗盐提纯”的实验中,操作步骤为溶解-过滤-蒸发-转移,在溶解、过滤、蒸发、转移操作中都要用到的玻璃仪器是玻璃棒;在溶解操作中玻璃棒的作用是搅拌,加快溶解;在过滤操作中玻璃棒的作用是引流;蒸发时玻璃棒的作用是搅拌,防止局部温度过高,造成液滴飞溅;在转移食盐固体的操作中玻璃棒的作用是转移固体.
(6)生成沉淀的质量是:100g+100g-156.95g=43.05g
设100“卤水”中氯化钠的质量是x
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
x 43.05 g
| 58.5 |
| x |
| 143.5 |
| 43.05g |
x=11.55g
则该卤水中氯化钠的质量分数是:
| 11.55g |
| 100g |
答:则该卤水中氯化钠的质量分数是11.55%.
(7)碱与盐反应,生成氯化钠的反应方程式是:2NaOH+CuCl2═2NaCl+Cu(OH)2↓
盐与盐反应,生成氯化钠的反应方程式是:Na2CO3+BaCl2=2NaCl+BaCO3↓.
故答案为:(1)隔离可燃物;降温至可燃物的着火点以下.
(2)加明矾使杂质沉降;用活性炭吸附除杂、除异味;通过煮沸来消毒等.
(3)油脂、蛋白质.
(4)钠离子和氯离子.
(5)加速溶解、引流、防止液体局部过热.
(6)11.55%.
(7)2NaOH+CuCl2═2NaCl+Cu(OH)2↓;Na2CO3+BaCl2=2NaCl+BaCO3↓.
点评:掌握化学方程式的计算格式和规范性,并能根据题目所给信息细心分析解答是解题的关键.

练习册系列答案
相关题目
按下列装置实验,不能达到对应目的是( )
A、 收集H2 |
B、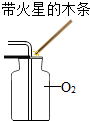 O2验满 |
C、 配制20%的Ca(OH)2溶液 |
D、 除去CO中的CO2 |
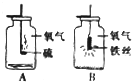 A,B两图分别表示硫、铁丝在氧气中燃烧的示意图.
A,B两图分别表示硫、铁丝在氧气中燃烧的示意图. 牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,对人体安全的一种日用必需品.某研究性学习小组对某一品牌牙膏中所含摩擦剂的成分及含量进行了如下探究.
牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,对人体安全的一种日用必需品.某研究性学习小组对某一品牌牙膏中所含摩擦剂的成分及含量进行了如下探究.
 现有A~G七种物质,已知A是赤铁矿的主要成分,B是一种气体,E的浓溶液加水稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系:
现有A~G七种物质,已知A是赤铁矿的主要成分,B是一种气体,E的浓溶液加水稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系: