题目内容
把一定量的锌放入过量的稀硫酸中,溶液的质量 (填增加或减少或不变),剩余液体中,溶质是 ,溶剂是 .
考点:金属的化学性质,溶液、溶质和溶剂的相互关系与判断
专题:金属与金属材料
分析:根据把一定量的锌放入过量的稀硫酸中,锌会和稀硫酸反应产生硫酸锌和氢气,结合化学方程式的意义分析溶液的质量变化,根据反应发生情况,判断溶液的组成.
解答:解:把一定量的锌放入过量的稀硫酸中,其中锌会和稀硫酸反应产生硫酸锌和氢气,反应的方程式为:Zn+H2SO4═ZnSO4+H2↑
65 2
通过锌和硫酸的反应关系可知,反应65份的锌产生2份的氢气,因此溶液的质量增加;由于反应后产生硫酸锌,因此溶质含有硫酸锌,且稀硫酸过量,因此还含有硫酸,即反应后的溶液中的溶质是硫酸锌和硫酸;溶剂稀硫酸中没有反应的水;
故答案为:增加;硫酸锌和硫酸;水.
65 2
通过锌和硫酸的反应关系可知,反应65份的锌产生2份的氢气,因此溶液的质量增加;由于反应后产生硫酸锌,因此溶质含有硫酸锌,且稀硫酸过量,因此还含有硫酸,即反应后的溶液中的溶质是硫酸锌和硫酸;溶剂稀硫酸中没有反应的水;
故答案为:增加;硫酸锌和硫酸;水.
点评:本题考查了金属和酸的反应,把握反应的程度及反应的原理结合反应方程式的意义是解题的关键.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
 符合图示从属关系的是( )
符合图示从属关系的是( ) | A | B | C | D | |
| X | 金属 | 溶液 | 浓溶液 | 游离态 |
| Y | 单质 | 乳浊液 | 饱和溶液 | 化合态 |
| A、A | B、B | C、C | D、D |
下列实验操作中,正确的是( )
A、 过滤 |
B、 熄灭酒精灯 |
C、 滴加试剂 |
D、 读取液体体积 |
下列有关物质的检验或区分方法中不正确的是( )
| A、鉴别铁粉和石墨粉时,分别加入稀盐酸,若有气体放出,则证明为铁粉 |
| B、若要除去硫酸铁溶液中混有的稀硫酸,可以往其中加入过量的氧化铁粉末 |
| C、向某物质中加入稀盐酸,有无色气体放出,则证明该物质是碳酸盐 |
| D、某化肥与碱共热,若产生使湿润红色石蕊试纸变蓝的气体,证明为铵态氮肥 |
能正确反映对应变化关系的图象是( )
A、 加热一定质量的高锰酸钾固体 |
B、 向一定量的稀硫酸中不断加镁条至过量 |
C、 一定温度下,向不饱和硝酸钠溶液中不断加入硝酸钠固体,充分搅拌 |
D、 分别向同质量,同质量分数的稀硫酸中不断加入镁和锌固体 |
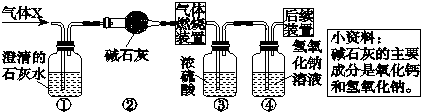
某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种.为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g.下列关于气体X成分的分析中,正确的是( )

| A、可能有二氧化碳 |
| B、可能同时含有甲烷和氢气 |
| C、不可能只有甲烷 |
| D、可能含有氢气和一氧化碳 |