题目内容
某同学为了测定蛋壳中碳酸钙的含量,12.5克蛋壳样品,经粉碎后放入烧杯中,并加入足量的稀盐酸(蛋壳中的杂质不与稀盐酸反应),直到没有气泡产生.测得加入的盐酸质量为100克,反应完成后,测得烧杯中所盛物质的质量为108.1克.求:
(1)反应生成CO2的总质量为 克.
(2)该蛋壳样品中碳酸钙的质量分数是多少?
(1)反应生成CO2的总质量为
(2)该蛋壳样品中碳酸钙的质量分数是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据反应前后的质量差即为反应生成二氧化碳的质量,通过二氧化碳的质量可以计算碳酸钙的质量,进一步可以计算该鸡蛋壳中碳酸钙的质量分数.
解答:解:(1)依据质量守恒定律可知,反应生成二氧化碳的质量为:100g+12.5g-108.1g=4.4g;
(2)设碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4.4g
=
x=10g,
所以该鸡蛋壳中碳酸钙的质量分数为:
×100%=80%,
答:该鸡蛋壳中碳酸钙的质量分数为80%.
故答案为:(1)4.4g;
(2)该蛋壳样品中碳酸钙的质量分数是80%.
(2)设碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
x=10g,
所以该鸡蛋壳中碳酸钙的质量分数为:
| 10g |
| 12.5g |
答:该鸡蛋壳中碳酸钙的质量分数为80%.
故答案为:(1)4.4g;
(2)该蛋壳样品中碳酸钙的质量分数是80%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
生活中属于物理变化的是( )
| A、冰雪消融 | B、大米酿酒 |
| C、蜡烛燃烧 | D、动物呼吸 |
2014年南京青奥会火炬使用的燃料为A物质,纯净物A在B物质中充分燃烧,发生反应:A+5B
3C+4D(部分微观示意图如下所示)
下列说法不正确的是( )
| ||
| 物质 | A | B | C | D | 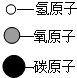 |
| 分子示意图 | ? |  |  |  |
| A、A物质中含有碳、氢、氧三种元素 |
| B、A物质中含有碳、氢原子个数比为3:8 |
| C、A物质具有可燃性,B物质具有氧化性 |
| D、该反应既不是化合反应也不是分解反应 |
下列化学用语表示正确的是( )
| A、2个氢分子-2H | ||
| B、3个氧原子-O3 | ||
| C、水分子-H2O2 | ||
D、+1价钠元素-
|
 甲乙丙三种固体物质的溶液度曲线如图所示,
甲乙丙三种固体物质的溶液度曲线如图所示, 鸡蛋壳主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半.试计算(计算结果保留1位小数):(盐酸是HCl溶于水形成的溶液,反应中水不参加反应)
鸡蛋壳主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半.试计算(计算结果保留1位小数):(盐酸是HCl溶于水形成的溶液,反应中水不参加反应)