题目内容
16.250吨含Fe2O3的质量分数为80%的赤铁矿石,如果在冶炼过程中损失矿石5%,则可炼出含铁的质量分数为98%的生铁多少吨?分析 由赤铁矿石的质量、氧化铁的质量分数、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
解答 解:能用于炼铁的赤铁矿石的质量为:250t×(1-5%)=237.5t
设理论上可以炼出含铁98%的生铁的质量为x.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
237.5t×80% 98%x
$\frac{160}{112}=\frac{237.5t×80%}{98%x}$ 解得:x≈135.7t
答:可炼出含铁98%的生铁135.7t.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键

练习册系列答案
相关题目
7.为研究重金属镉(Cd)对种子萌发的影响,科学家选用均匀一致的同种玉米种子,经过消毒、无菌水冲洗处理后,分八个组实验.每一组取10粒玉米种子,在培养皿中用某一浓度的Cd2+(试剂选用的是硫酸镉CdSO4)的营养液培养并置于室温下,每一组做3次实验.培养7天后统计发芽率,各组取平均值,结果如下表:

(1)实验中培养皿里放10粒玉米种子而不是1粒,每组都做3次实验,其目的避免偶然性.
(2)Cd2+处于何浓度时,对玉米种子的萌发有明显的抑制作用?大于50.
(3)大量含镉的固体废弃物或污水会造成土壤污染.溶解在土壤中的镉会被植物吸收,并通过食物链进一步富集并进入人体,对人体造成多种危害.
(4)为保护环境,实验所用的硫酸镉是不能随意排放的,下面是某处理方法中的一个重要反应:CdSO4+Na2S═CdS↓+Na2SO4,该化学反应的基本类型是复分解反应.
(5)“mg/L”为溶液浓度的一种单位,读作“毫克每升”.现取Cd2+浓度为50mg/L的溶液200毫升,加水稀释至1升,稀释后溶液的Cd2+浓度为10mg/L.

| 组别 | 一 | 二 | 三 | 四 | 五 | 六 | 七 | 八 |
| 镉(Cd2+)浓度(mg/L) | 0 | 5 | 10 | 15 | 30 | 50 | 100 | 120 |
| 发芽率(%) | 95.0 | 96.7 | 97.2 | 98.0 | 95.4 | 74.5 | 55.4 | 0 |
(2)Cd2+处于何浓度时,对玉米种子的萌发有明显的抑制作用?大于50.
(3)大量含镉的固体废弃物或污水会造成土壤污染.溶解在土壤中的镉会被植物吸收,并通过食物链进一步富集并进入人体,对人体造成多种危害.
(4)为保护环境,实验所用的硫酸镉是不能随意排放的,下面是某处理方法中的一个重要反应:CdSO4+Na2S═CdS↓+Na2SO4,该化学反应的基本类型是复分解反应.
(5)“mg/L”为溶液浓度的一种单位,读作“毫克每升”.现取Cd2+浓度为50mg/L的溶液200毫升,加水稀释至1升,稀释后溶液的Cd2+浓度为10mg/L.
4.某同学对酸碱盐的知识进行了以下梳理
(1)请根据下表盐中的金属元素的排列顺序,填写空格中的化学式:
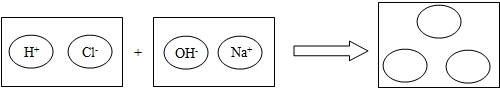
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在如图的圆圈中填入适当的化学式或离子符号应该是H2O,Na+,Cl-.
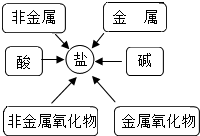
(3)此同学通过查阅资料,发现许多反应都有盐类物质生成(如图).比如①用稀硫酸除铁锈;②古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液,①、②中任选一个,写出反应的化学方程式:Fe+CuSO4═FeSO4+Cu(或Fe2O3+3H2SO4═Fe2(SO4)3+3H2O).
(1)请根据下表盐中的金属元素的排列顺序,填写空格中的化学式:
| KNO3 | Ca(NO3)2 | Na(NO3)2 | Mg(NO3)2 | Al(NO3)3 | Zn(NO3)2 | Fe(NO3)2 |

(3)此同学通过查阅资料,发现许多反应都有盐类物质生成(如图).比如①用稀硫酸除铁锈;②古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液,①、②中任选一个,写出反应的化学方程式:Fe+CuSO4═FeSO4+Cu(或Fe2O3+3H2SO4═Fe2(SO4)3+3H2O).

11.下列不是实验室制取氧气所用方法的是( )
| A. | 加热高锰酸钾 | B. | 用二氧化锰和双氧水 | ||
| C. | 用直流电电解水 | D. | 加热氯酸钾和二氧化锰的混合物 |
1.下列除去杂质的方法中,正确的是( )
| 物质 | 杂质 | 除杂质的试剂和方法 | |
| A | NaOH | Na2CO3 | 加入适量的稀盐酸,蒸发 |
| B | CaO | CaCO3 | 高温煅烧后冷却 |
| C | FeCl2 | CuCl2 | 溶解,过滤,蒸发 |
| D | Zn | Cu | 加入足量稀盐酸后过滤 |
| A. | A | B. | B | C. | C | D. | D |
6.为验证A、B、C三种金属的活动性,将它们分别投入稀盐酸中,只有C不能与盐酸作用产生气体.再把A投入B的硝酸盐溶液中,在A的表面有B析出.则三种金属的活动性顺序为( )
| A. | B>A>C | B. | A>B>C | C. | B>C>A | D. | C>A>B |
 有媒体曝出深圳部分居民楼墙体裂缝等问题,据调查是建设时违规使用氯离子超标的海砂,严重腐蚀混凝土里的钢筋.国家标准要求海砂中氯离子的含量必须低于0.3%.为了测定某工地海砂中氯离子的含量,某校科学兴趣小组进行了如下实验:取固体海砂样品2840g,全部溶于水中(假设氯离子都存在于氯化钠中),加入一定质量分数的硝酸银溶液,产生沉淀的量与加入溶液的量如图所示,请回答:
有媒体曝出深圳部分居民楼墙体裂缝等问题,据调查是建设时违规使用氯离子超标的海砂,严重腐蚀混凝土里的钢筋.国家标准要求海砂中氯离子的含量必须低于0.3%.为了测定某工地海砂中氯离子的含量,某校科学兴趣小组进行了如下实验:取固体海砂样品2840g,全部溶于水中(假设氯离子都存在于氯化钠中),加入一定质量分数的硝酸银溶液,产生沉淀的量与加入溶液的量如图所示,请回答: