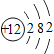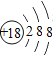题目内容
【题目】在密闭容器内加入氧气、二氧化碳、水蒸气和一种未知物质 W,在一定条件下充分反应,测得反应前后各物质的质量如下表所示。下列说法中正确的是
物质 | 氧气 | 二氧化碳 | 水蒸气 | W |
反应前质量/g | 50 | 1 | 1 | 23 |
反应后质量/g | 2 | 45 | 28 | x |
A.x的值应为2
B.该反应可能是分解反应
C.反应中的氧气和二氧化碳的质量比为25:22
D.w物质中碳元素的质量等于二氧化碳中碳元素的质量
【答案】D
【解析】
根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和。反应后质量增加的是生成物,减少的是反应物,由表格信息可知反应后CO2质量增加了45g-1g=44g,是生成物;H2O质量增加了28g-1g=27g,是生成物;O2质量减少了50g -2g=48g,是反应物;反应后的质量还少50g+1g+1g+23g=2g+45g+28g+![]() ,得
,得![]() =0g,所以反应后物质W的质量x为0,所以W是反应物,反应物是W和O2,生成物是CO2 和 H2O,根据反应前后元素种类不变,生成物中含有C,H和O三种元素,反应物O2中含有O元素。所以C和H一定来自W。
=0g,所以反应后物质W的质量x为0,所以W是反应物,反应物是W和O2,生成物是CO2 和 H2O,根据反应前后元素种类不变,生成物中含有C,H和O三种元素,反应物O2中含有O元素。所以C和H一定来自W。
根据以上分析可知:
A、由质量守恒定律可知,化学反应前后物质的总质量不变,![]() =0g,故选项错误;
=0g,故选项错误;
B、由反应前后物质的质量变化情况可知,反应物是W和O2,生成物是CO2 和 H2O,不符合分解反应的特征,故选项错误;
C、反应中的氧气和二氧化碳的质量比为48g:44g =12:11,故选项错误;
D、该反应的生成物是二氧化碳和水,水中不含碳元素,由质量守恒定律可知,W中碳元素的质量等于二氧化碳中碳元素的质量,故选项正确。故选D。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】下表为元素周期表中某一周期元素的原子结构示意图。请回答下列问题:
元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | |
元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
原子结构示意图 |
|
|
|
|
|
|
|
|
(1)镁原子的核电荷数是____ 。
(2)氯原子在化学反应中容易_____ (填“得到”或“失去”)电子。
(3)从原子结构角度分析,上述元素位于同一周期的原因是____ 。